


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
| A、K+、H+、SO42-、OH- |
| B、Na+、H+、Cl-、CO32- |
| C、Na+、Ca2+、NO3-、CO32- |
| D、Na+、Cu2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 燃煤废气中的氮氧化物(NO)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.
燃煤废气中的氮氧化物(NO)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.
| ||
| m(H2) |
| n(CO2) |
| 1 |
| 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 高温高压 |
查看答案和解析>>
科目:高中化学 来源: 题型:
139 57 |
59 28 |
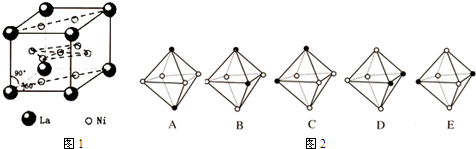
查看答案和解析>>
科目:高中化学 来源: 题型:

| A |
| S |
| A |
| S |
| A |
| S |
| A |
| S |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、13g乙炔和苯的混合液中总原子数为2NA |
| B、4℃时9mL水和11.2L氮气含有相同的分子数 |
| C、同温同压下,NA个NO2与NA个N2和O2的混合气体的体积不相等 |
| D、1.01×105Pa时,11.2 L氧气所含的原子数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com