
水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C(s) + H2O(g) CO(g) +H2(g) △H=+131.3 kJ·mol-1
CO(g) +H2(g) △H=+131.3 kJ·mol-1
(1)该反应的平衡常数K随温度的升高而___________(选填“增大”“ 减小”或“不变”)
(2)上述反应达到平衡后,将体系中的C(s)部分移走,平衡____________(选填“向左移”“向右移”或“不移动”)。
(3)下列事实能说明该反应在一定条件下已达到平衡状态的有___________(填序号)。
A.单位体积内每消耗1 mol CO的同时生成1molH2
B.混合气体总物质的量保持不变
C.生成H2O(g)的速率与消耗CO的速率相等
D.H2O(g)、CO、H2的浓度相等
(4)某温度下,将4.0 mol H2O(g)和足量的炭充入2 L的密闭容器中,发生如下反应,C(s)+ H2O(g) CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为________________。
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为________________。
(5)己知:① C(s)+H2O(l) CO(g)+H2(g) △H1
CO(g)+H2(g) △H1
② 2CO(g)+O2(g)=2CO2 (g) △H2
③ H2O (l)=H2 (g)+1/2 O2 (g) △H3
则C(s)+O2 (g)=CO2 (g)的△H=_____________________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2015-2016学年福建省高二下学期期末化学试卷(解析版) 题型:选择题
用纤维素为主要原料制备乙酸乙酯的路线如下:
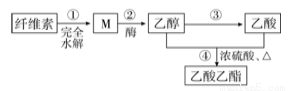
下列说法正确的是( )
A.若用淀粉替代纤维素,一定条件下也能按照此路线制备乙酸乙酯
B.M虽然分子结构中无醛基,但仍然可以发生银镜反应
C.步骤②,1molM完全反应可以生成3mol乙醇
D.③和④都发生了氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南师大附中高一下学期末化学试卷(解析版) 题型:填空题
A、B、C、D为短周期元素,核电荷数依次增大,且A、B、C三种元素的原子核外电子层数之和为5。已知A是原子结构最简单的元素;B元素原子最外层上的电子数是其电子层数的2倍;A和C之间可形成A2C和A2C2两种化合物;D在同周期主族元素中原子半径最大,请回答下列问题。
(1)C元素在元素周期表中的位置是____________;写出BC2的结构式__________。
(2)C、D两种元素所形成的简单离子,半径由大到小的顺序是________________。(用离子符号表示)
(3)在恒温下,体积为2 L的恒容容器中加入一定量的B单质和1 mol A2C蒸汽,发生:B(s)+A2C(g)  BC(g)+A2(g)。2 min后,容器的压强增加了20%,则2 min内A2C的反应速率为__________。一段时间后达到平衡,下列说法正确的是__________。
BC(g)+A2(g)。2 min后,容器的压强增加了20%,则2 min内A2C的反应速率为__________。一段时间后达到平衡,下列说法正确的是__________。
A.增加B单质的量,反应速率加快
B.恒温恒容时在该容器中通入Ar,反应速率加快
C.气体的密度不再变化可以判断该反应达到了平衡
D.2 min时,A2C的转化率为80%
E.气体的平均摩尔质量不变时,该反应达到平衡
(4)BC与C2在DCA溶液中可形成一种燃料电池。该电池的负极反应式为:
________________________________________________________________________。
(5)写出D的单质与乙醇反应的化学方程式:
________________________________________________________________________。
(6)将0.2 mol D2C2投入到含有0.1 mol FeCl2的水溶液中恰好充分反应,反应的总的化学方程式为:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省眉山市高二下学期期末理综化学试卷(解析版) 题型:简答题
锰的单质及其化合物在生产、生活中有广泛应用。
(1)碱性锌锰电池广泛应用于日常生活。电池的总反应式为:Zn(s)+2MnO2(s)+2H2O(l)===Zn(OH)2(s)+2MnOOH(s)。该电池的正极反应式为 。
(2)某学习小组拟以废旧干电池为原料制取锰,简易流程如下:
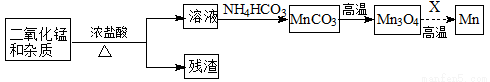
①加入浓盐酸溶解废旧电池内黑色物质过程中保持通风,其原因是 。
②从产品纯度、环保等角度考虑,X宜选择 (填代号)。
A.焦炭 B.铝 C.氢气 D.一氧化碳
③写出碳酸锰在空气中灼烧生成四氧化三锰的化学方程式 。
(3)电解硫酸锰溶液法制锰又叫湿法冶锰。以菱锰矿(主要成份是MnCO3,主要杂质是Fe2+、Co2+、Ni2+)为原料制备锰的工艺流程如下:

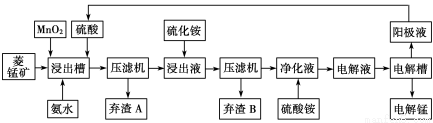
已知:NiS 、CoS均难溶于水。部分氢氧化物的pH如下表:(若某离子浓度小于等于10?5mol·L?1,则认为完全沉淀)
物质 | Fe(OH)2 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 | Fe(OH)3 |
开始沉淀pH | 7.5 | 7.7 | 7.6 | 8.3 | 2.7 |
完全沉淀pH | 9.7 | 8.4 | 8.5 | 9.8 | 3.8 |
①浸出槽内MnO2的作用是(用离子方程式表示) 。
②加入氨水调节浸出槽中溶液的pH范围为 。
③电解槽阴极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省眉山市高二下学期期末理综化学试卷(解析版) 题型:选择题
下列实验“操作和现象”与“结论”都正确的是( )
选项 | 操作和现象 | 结 论 |
A | 向盛有2mL 0.1mol/L AgNO3溶液的试管中,先滴几滴0.1mol/L KCl溶液,再滴加0.1mol/L KI溶液。试管中先出现白色沉淀,后出现淡黄色沉淀 | Ksp(AgCl)< Ksp(AgI) |
B | 在分液漏斗中加入碘水后再加入CCl4,充分振荡,静置分层,下层溶液呈紫色 | CCl4可作为碘的萃取剂 |
C | 向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4溶液颜色基本不变 | Fe(NO3)2与H2SO4不反应 |
D | 测定饱和NaClO溶液、CH3COONa溶液的pH, pH(NaClO)> pH(CH3COONa) | 弱酸的酸性: HClO >CH3COOH |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省天门、仙桃、潜江市高一下学期期末化学试卷(解析版) 题型:选择题
下列事实中,不能用勒夏特列原理解释的是
A.冰镇的啤酒打开后泛起泡沫
B.对N2+3H2 2NH3的反应,使用铁触媒可加快合成氨反应的速率
2NH3的反应,使用铁触媒可加快合成氨反应的速率
C.工业制取金属钾Na(l)+KCl(l) NaCl(l)+K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省天门、仙桃、潜江市高一下学期期末化学试卷(解析版) 题型:选择题
下列变化中可以说明SO2具有漂白性的是
A.SO2通入高锰酸钾酸性溶液中紫色褪去
B.SO2通入品红溶液中红色褪去
C.SO2通入溴水溶液中红棕色褪去
D.SO2通入氢氧化钠与酚酞的混合溶液中红色褪去
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省天门、仙桃、潜江市高二下学期期末化学试卷(解析版) 题型:选择题
常温下,下列溶液的离子浓度关系式正确的是
A.pH=4的氯化铵溶液中:c(H+)= c(NH3·H2O )=1×10-4mol·L-1
B.pH=a的HCl溶液,稀释10倍后,其pH=b,则a=b-1
C.pH=2的HF溶液与pH=12的NaOH溶液以体积比1:1混合:c(Na+)=c(F-)>c(H+)=c(OH-)
D.pH相同的①NaOH、②NaClO两种溶液中水的电离程度:①<②
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高一下学期期末化学试卷(解析版) 题型:选择题
如图所示是元素周期表前六周期的一部分,关于元素X、Y、Z的叙述正确的是( )
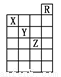
①X的气态氢化物与Y的最高价氧化物对应的水化物能发生反应生成盐
②X、Y、Z的气态氢化物的水溶液的酸性X<Y<Z
③Z的单质在常温下是液体,可与铁粉反应
④Z的原子序数比Y大19
⑤Z所在的周期中含有32种元素
A. 只有③ B. ①④ C. ①②③④ D. ①②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com