

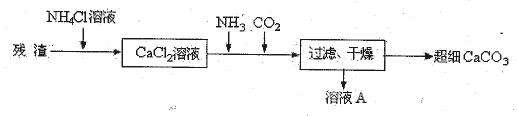
 Ca2++CO32-,NH4Cl溶液显酸性,使CO32-浓度减小,平衡向右移动,CaCO3溶解(或其他合理答案) (2分)
Ca2++CO32-,NH4Cl溶液显酸性,使CO32-浓度减小,平衡向右移动,CaCO3溶解(或其他合理答案) (2分) Ca2++CO32-,而NH4Cl溶液水解产生的H+
Ca2++CO32-,而NH4Cl溶液水解产生的H+

 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源:不详 题型:单选题
A.实验室制取乙烯的反应原理:C2H5OH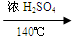 C2H4 ↑+ H2O C2H4 ↑+ H2O |
| B.实验室制取C2H2,一般用碳化钙跟饱和食盐水反应以适度减缓反应速率 |
| C.实验室分离苯和苯酚的混合物,可采用溴水 |
| D.由1—溴丁烷跟氢氧化钠醇溶液共热,可以制得两种烯烃 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
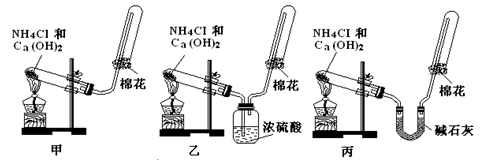
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
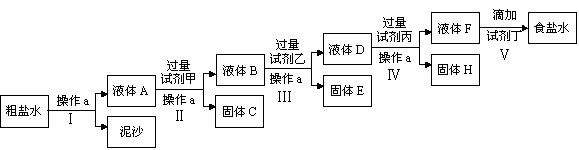 请回答以下问题:
请回答以下问题:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
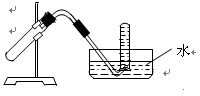
| A.加热NaHCO3固体制CO2 |
| B.Cu和稀HNO3反应制NO |
| C.NH4Cl与浓Ca(OH)2溶液反应制NH3 |
| D.Cu和浓HNO3反应制NO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
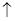 +8H2O
+8H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com