
 有机物X的键线式为:
有机物X的键线式为: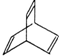
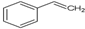
 .
. 分析 (1)由有机物X的键线式为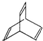 可知,X的分子式为C8H8,其不饱和度为=$\frac{8×2+2-8}{2}$=5,一个苯环的不饱和度是4,有机物Y是X的同分异构体,所以属于芳香烃的Y中除了有一个苯环外还有一个碳碳双键,据此可写出结构简式;
可知,X的分子式为C8H8,其不饱和度为=$\frac{8×2+2-8}{2}$=5,一个苯环的不饱和度是4,有机物Y是X的同分异构体,所以属于芳香烃的Y中除了有一个苯环外还有一个碳碳双键,据此可写出结构简式;
(2) 与足量的H2在一定条件下反应可生成环状的饱和烃为
与足量的H2在一定条件下反应可生成环状的饱和烃为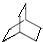 ,据此写它的一氯代物的结构简式;
,据此写它的一氯代物的结构简式;
(3)苯乙烯含有碳碳双键,通过加成聚合生成聚苯乙烯.
解答 解:(1)由有机物X的键线式为 可知,X的分子式为C8H8,其不饱和度=$\frac{8×2+2-8}{2}$=5,一个苯环的不饱和度是4,有机物Y是X的同分异构体,所以属于芳香烃的Y中除了有一个苯环外还有一个碳碳双键,所以Y的结构简式为
可知,X的分子式为C8H8,其不饱和度=$\frac{8×2+2-8}{2}$=5,一个苯环的不饱和度是4,有机物Y是X的同分异构体,所以属于芳香烃的Y中除了有一个苯环外还有一个碳碳双键,所以Y的结构简式为 ,
,
故答案为: ;
;
(2) 与足量的H2在一定条件下反应可生成环状的饱和烃为
与足量的H2在一定条件下反应可生成环状的饱和烃为 ,它的一氯代物有
,它的一氯代物有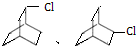 ,共2种,
,共2种,
故答案为:2;
(3)苯乙烯发生加成聚合反应的化学方程式为: ;故答案为:
;故答案为: .
.
点评 本题主要考查根据条件书写同分异构体,难度不大,答题时注意有机结构基础知识的运用.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④ | C. | ①② | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x>a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x>b | 电极附近出现黄色,无气泡产生 | 有Fe3+,无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+,无Cl2 |
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x>c | 无明显变化 | 有Cl2 |
| Ⅴ | c<x<b | 无明显变化 | 无Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应 | |
| B. | 食醋的主要成分是醋酸,将一定量的醋酸溶液稀释,溶液中各离子的浓度都减小 | |
| C. | 味精的主要成分是谷氨酸钠,向其中加入盐酸可得谷氨酸,谷氨酸具有两性 | |
| D. | 木糖醇(C5H12O5)是一种甜味剂,它属于多羟基化合物,与葡萄糖互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com