
【题目】下表为元素周期表的一部分,表中列出12种元素在周期表中的位置,按要求回答下列各题:
周期族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | |||||||
2 | ⑦ | ⑨ | ||||||
3 | ② | ④ | ⑥ | ⑧ | ⑩ | |||
4 | ③ | ⑤ |
(1)这12种元素中,化学性质最不活泼的元素是______(填元素符号或化学式,下同),得电子能力最强的原子是______,失电子能力最强的单质与水反应的离子反应方程式是____,常温下单质为液态的非金属单质是____________。
(2)元素⑤的离子结构示意图为__________________。
(3)写出⑦⑧⑨与①形成的简单化合物中最稳定的分子式________。写出⑧⑩两种元素最高价氧化物对应水化物中酸性较弱的化学式________。
(4)写出⑨⑩与①形成的化合物中沸点最低的化学式______酸性最强的化学式_______。
(5)写出④的单质置换出⑦的单质的化学反应方程式:__________________。
②和⑥两种元素最高价氧化物对应的水化物相互反应的离子方程式为__________。
③和⑩两种元素最高价氧化物对应的水化物相互反应的离子方程式为__________。
用电子式表示⑤与⑨组成的二元化合物的形成过程_____________________。
【答案】Ne F 2K+2H2O=2K++H2↑+2OH- Br2 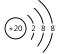 HF H3PO4 HCl HBr 2Mg+CO2
HF H3PO4 HCl HBr 2Mg+CO2![]() 2MgO +C OH-+Al(OH)3=AlO2-+2H2O OH-+H+=H2O
2MgO +C OH-+Al(OH)3=AlO2-+2H2O OH-+H+=H2O ![]()
【解析】
根据元素周期表的结构可知,①②③④⑤⑥⑦⑧⑨⑩分别是H、Na、K、Mg、Ca、Al、C、P、F、Cl、Br、Ne,结合元素周期表与元素周期律进行回答。
根据上述分析可知,
(1)这12种元素中,化学性质最不活泼的元素是Ne;同周期从左向右元素的金属性逐渐减弱、非金属逐渐增强,同主族从上向下元素的金属性逐渐增强、非金属性逐渐减弱,非金属性越强得电子能力越强,则得电子能力最强的是F,失电子能力最强的单质为K,K与水反应的离子反应方程式是2K+2H2O=2K++H2↑+2OH-,常温下单质为液态的非金属单质是Br2,
故答案为:Ne;F;2K+2H2O=2K++H2↑+2OH-;Br2;
(2)元素⑤为Ca,核电荷数为20,则Ca2+的结构示意图为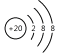 ,
,
故答案为: ;
;
(3)写出⑦⑧⑨与①形成的简单化合物中分别是CH4、PH3和HF,元素的非金属性越强,则对应气态氢化物的稳定性越好,则最稳定的分子式是HF;⑧⑩两种元素最高价氧化物对应水化物分别为磷酸与高氯酸,因非金属性P<Cl,则酸性较弱的化学式是H3PO4,
故答案为:HF;H3PO4;
(4)⑨⑩与①形成的化合物分别是HF、HCl和HBr,三者均属于分子晶体,但HF分子间存在氢键,HF熔沸点最高,HCl和HBr比较,其熔沸点随相对分子质量的增大而增大,故沸点最低的化学式为HCl;HF为弱酸,HCl和HBr为强酸,且酸性HCl<HBr,酸性最强的是HBr,
故答案为:HCl;HBr;
(5)Mg可与二氧化碳发生反应置换出C单质,其化学方程式为:2Mg+CO2![]() 2MgO +C;②和⑥两种元素最高价氧化物对应的水化物分别是氢氧化钠与氢氧化铝,两者相互反应的离子方程式为OH-+Al(OH)3=AlO2-+2H2O;③和⑩两种元素最高价氧化物对应的水化物分别为氢氧化钾与HClO4,两者相互反应的离子方程式为:OH-+H+=H2O;⑤与⑨组成的二元化合物为氟化钙,是离子化合物,用电子式表示CaF2的形成过程为
2MgO +C;②和⑥两种元素最高价氧化物对应的水化物分别是氢氧化钠与氢氧化铝,两者相互反应的离子方程式为OH-+Al(OH)3=AlO2-+2H2O;③和⑩两种元素最高价氧化物对应的水化物分别为氢氧化钾与HClO4,两者相互反应的离子方程式为:OH-+H+=H2O;⑤与⑨组成的二元化合物为氟化钙,是离子化合物,用电子式表示CaF2的形成过程为![]() ,
,
故答案为:2Mg+CO2![]() 2MgO+C;OH-+Al(OH)3=AlO2-+2H2O;OH-+H+=H2O;
2MgO+C;OH-+Al(OH)3=AlO2-+2H2O;OH-+H+=H2O;![]() 。
。


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】判断下列粒子的空间构型
(1)CO2:_______________________
(2)H2S:____________
(3)SO2:___________
(4)NH4+:_________________
(5)CO32-:_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质及对应用途描述正确的是( )
A.SO2具有氧化性,可用于纸浆漂白
B.金属镁燃烧时会发出耀眼的白光,常用作耐高温材料
C.碳酸钠溶液显碱性,可用于清洗油污
D.浓硫酸具有脱水性,可用作干燥剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿波罗宇宙飞船以N2H4(联氨)和N2O4为推力源,反应温度达2 700 ℃,反应式为2N2H4+N2O4=3N2+4H2O,关于该反应的说法中正确的是( )
A.属于置换反应B.联氨是氧化剂
C.联氨是还原剂D.氮气是氧化产物,不是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z和W代表原子序数依次增大的四种短周期主族元素.它们满足以下条件:①在元素周期表中,Z与Y、W均相邻;②X、Y、W分别位于不同周期;③Y、Z、W三种元素的原子最外层电子数之和为17。下列说法错误的是
A. X、Y、Z既能形成离子化合物,又能形成共价化合物
B. Y和Z元素的原子半径大小顺序为Y>Z
C. X与Y、Z之间形成的核外电子总数为10的微粒只有YX3和X2Z
D. Z、W元素的最简单氢化物的沸点和稳定性均为H2Z>H2W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某碳酸钠和碳酸氢钠的混合物跟足量盐酸反应,消耗H+和产生CO2的物质的量之比为5:4,该混合物中碳酸钠和碳酸氢钠的物质的量之比为
A.1:3B.2:3C.3:4D.4:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1.20 g铁铜合金完全溶于100 mL、12.0 mol·L-1浓硝酸中,得到NO2和N2O4混合气体672 mL(换算为标准状况下)。向反应后的溶液中加入1.0 mol·L-1 NaOH溶液,当金属离子全部沉淀时,得到2.05 g沉淀。下列有关判断正确的是
A. 反应过程中浓硝酸仅体现氧化性
B. 该合金中铁与铜物质的量之比是2∶1
C. 混合气体中,NO2的体积分数是1/3
D. 金属离子全部沉淀时,加入NaOH溶液的体积至少为1150 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4既是一种重要的能源,也是一种重要的化工原料。
(1)已知8.0 g CH4完全燃烧生成液态水放出444.8 kJ热量。则CH4 (g)+2O2(g)=CO2(g)+2H2O(l) ΔH=____________kJ·mol-1。
(2)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示,则该反应的最佳温度应控制在 ___________左右。
②该反应催化剂的有效成分为偏铝酸亚铜 (CuAlO2,难溶物)。将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为 _____________________。

(3)CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下8.96 L CH4可处理22.4 L NOx,则x值为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一九二三年布朗特提出了酸碱质子理论,把酸碱概念加以推广。酸碱质子理论认为:凡是能够给出质子(H+)的物质都是酸、凡是能够接受质子的物质都是碱。下列微粒中,既可以看做酸又可以看做碱的是( )
A.NH4+B.CO32-C.S2-D.HCO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com