
【题目】金属钠是一种活泼金属,除了具有金属的一般性质外,还具有自己的特性。关于钠的叙述中,正确的是
A.钠是银白色金属,熔点低,硬度大
B.钠放置在空气中,会迅速被氧化而生成淡黄色的氧化钠
C.加热时,金属钠剧烈燃烧,产生黄色火焰
D.金属钠着火可以用泡沫灭火器或用干燥的沙土灭火
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案科目:高中化学 来源: 题型:
【题目】下列实验方案合理的是( )
A.向苯酚悬浊液中加入少量溴水制取三溴苯酚白色沉淀
B.用高锰酸钾溶液除去乙烯中混有的少量SO2
C.用水鉴别三种无色液体:苯、乙醇、四氯化碳
D.用蒸发的方法分离乙醇(沸点78.5℃)和乙醚(沸点34.5℃)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把0.6molX气体和0.4molY气体混合于2L容器中,使它们发生如下反应:3X(气)+Y(气)=nZ(气)+2W(气).5min末已生成0.2molW,若测知以Z浓度变化来表示的化学反应平均速率为0.01molL﹣1min﹣1 , 则上述反应中Z气体的计量系数 n的值是( )
A.1
B.2
C.3
D.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期主族元素原子半径与原子序数的关系.下列说法错误的是( ) 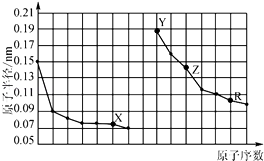
A.X,R的最高化合价相同
B.电解熔融的X与Z构成的化合物可以得到单质Z
C.X,Y形成的化合物中阳离子与阴离子的个数比一定是2:1
D.Y,Z,R对应的最高价氧化物的水化物相互之间可以发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将氢气和碘蒸气各1mol的气态混合物充入10L的密闭容器中.发生反应H2(g)+I2(g)=2HI(g).2分钟后达到平衡后.测得C(H2)=0.08molL﹣1 ,
(1)求该反应的平衡常数.
(2)求2分钟内的H2的反应速率.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验。
【实验1】铜与浓硫酸反应,实验装置如图所示。
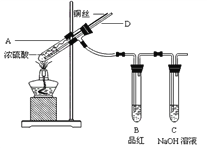
实验步骤:
①先连接好装置,检验气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面。
(1)装置 A 中发生反应的化学方程式为__________。实验中发现在 A 里产生了白色固体,其可能为________。C中NaOH溶液的作用为______
(2)熄灭酒精灯后,因为有导管D的存在,B中的液体不会倒吸,其原因是______。
(3)停止加热后,在拆除装置前,不需打开胶塞,就可使装置中残留气体完全被吸收,应当采取的操作是__________________。
【实验2】实验中发现试管A内除了产生白色固体外,在铜丝表面还产生黑色固体甲,其中可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧化亚铜。
查阅资料:
①氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,在氧气流中煅烧,可以转化为氧化铜。
②硫化铜和硫化亚铜常温下都不溶于稀盐酸,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫。
为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图所示的实验
(4)②中检验滤渣是否洗涤干净的实验操作是___________。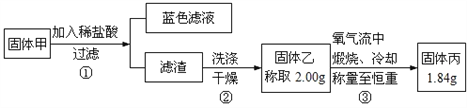
(5)③中在煅烧过程中一定发生的反应的化学方程式为_____________________。
(6)下列对于固体甲的成分的判断中,正确的是(填字母选项)____________。
A.固体甲中,CuS和Cu2S不能同时存在
B.固体甲中,CuO和Cu2O至少有一种
C.固体甲中若没有Cu2O,则一定有Cu2S
D.固体甲中若存在Cu2O,也可能有Cu2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液、胶体和浊液这三种分散系的根本区别是( )
A. 分散质粒子直径的大小B. 光束穿过胶体时形成一条光亮的通路
C. 能否透过滤纸或半透膜D. 是否均一、透明、稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中各含有少量的杂质,能用饱和Na2CO3溶液并借助于分液漏斗除去杂质的是( )
A.苯中含有少量甲苯
B.乙醇中含有少量乙酸
C.溴苯中含有少量苯
D.乙酸乙酯中含有少量的乙酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com