
| A. | K+、Cu2+、NO3-、SO42- | B. | K+、Na+、Cl-、ClO- | ||
| C. | Zn2+、NH4+、NO3-、Cl- | D. | K+、Na+、Ca2+、SO42- |
科目:高中化学 来源: 题型:选择题
| A. | ③④⑤ | B. | ①②③ | C. | ②④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极的反应式为:Zn2+-2e-=Zn | |
| B. | 正极反应式为2FeO42-+10H++6e-=Fe2O3+5H2O | |
| C. | 该电池放电过程中电解质溶液浓度不变 | |
| D. | 电池工作时OH-向负极迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | |
| Z | W |
| A. | X的氢化物可用作制冷剂 | |
| B. | Y与氢元素形成的物质中只含有极性共价键 | |
| C. | 4种元素的原子半径最大的是W | |
| D. | 4种元素中Z的最高价氧化物对应水化物的酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
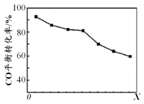 密闭容器中,由H2和CO直接制备二甲醚(CH3OCH3),其过程包含以下反应:
密闭容器中,由H2和CO直接制备二甲醚(CH3OCH3),其过程包含以下反应:| A. | 由H2和CO直接制备二甲醚的反应为放热反应 | |
| B. | 条件X为压强 | |
| C. | X增大,二甲醚的产率一定增大 | |
| D. | X增大,该反应的平衡常数一定减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 66 | 70 | 143 | 160 |
| 主要化合价 | -2 | +5、+3、-3 | +3 | +2 |
| A. | W和Y形成的化合物为共价化合物 | |
| B. | Y的最高价氧化物对应的水化物为强酸 | |
| C. | Y的简单气态氢化物的沸点高于X的简单气态氢化物 | |
| D. | 工业上经常采用电解Z的氯化物溶液制备Z单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2与O3互为同素异形体 | |
| B. | 35Cl与37Cl互为同位素,两者核外电子排布不同 | |
| C. | CH4与C3H8一定互为同系物 | |
| D. | CH3CH2NO2与H2NCH2COOH互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绿地可以保持水土,减少水土流失 | |
| B. | 绿地可以调节气候,减少空气中PM2.5含量 | |
| C. | 绿地可以吸收二氧化碳,转化生成氧气 | |
| D. | 为减少园林绿地中病虫害,大量使用杀虫剂解决问题 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3-甲基-1-丁烯的结构简式:(CH3)2CHCH=CH2 | |
| B. | 乙醇分子的比例模型: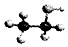 | |
| C. | CF2Cl2有两种同分异构体 | |
| D. | HOCH2COOH缩聚物的结构简式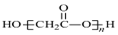 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com