
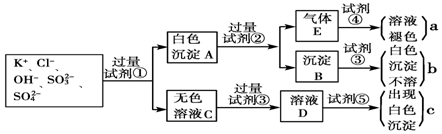
·ÖĪö SO32-”¢SO42-ÓėBa£ØNO3£©2ČÜŅŗ·“Ó¦·Ö±šÉś³ÉŃĒĮņĖį±µŗĶĮņĖį±µ°×É«³Įµķ£¬ŃĒĮņĖį±µÓėŃĪĖį·“Ӧɜ³É¶žŃõ»ÆĮņĘųĢ壬¶žŃõ»ÆĮņÄÜŹ¹äåĖ®ĶŹÉ«£¬¹ŹŹŌ¼Į¢ŁĪŖBa£ØNO3£©2ČÜŅŗ£¬ŹŌ¼Į¢ŚĪŖŃĪĖį£¬ŹŌ¼Į¢ÜĪŖäåĖ®£¬ŹŌ¼Į¢ŪĪŖĻõĖį£»ĪŽÉ«ČÜŅŗC³Ź¼īŠŌ£¬¼ÓČė¹żĮæĻõĖįµ÷ÕūČÜŅŗ³ŹĖįŠŌ£¬ŌŁ¼ÓČėŹŌ¼Į¢ŻĻõĖįŅųČÜŅŗ£¬Éś³ÉĀČ»ÆŅų°×É«³Įµķ£¬øł¾ŻŅŌÉĻ·ÖĪöæÉÖŖČÜŅŗÖŠŗ¬ÓŠCl-”¢SO32-”¢SO42-£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗ£Ø1£©ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬°×É«³ĮµķAÖŠŗ¬ĮņĖį±µ”¢ŃĒĮņĖį±µ£¬°×É«³ĮµķA¼ÓŹŌ¼Į¢Ś·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒBaSO3+2H+=Ba2++SO2”ü+H2O£¬
¹Ź“š°øĪŖ£ŗBaSO3+2H+=Ba2++SO2”ü+H2O£»
£Ø2£©ĪŽÉ«ČÜŅŗC¼ÓŹŌ¼Į¢ŪµÄÖ÷ŅŖÄæµÄŹĒÖŠŗĶOH-£¬·ĄÖ¹¶ŌCl-µÄ¼ģŃé²śÉśøÉČÅ£¬¹Ź“š°øĪŖ£ŗÖŠŗĶOH-£¬·ĄÖ¹¶ŌCl-µÄ¼ģŃé²śÉśøÉČÅ£»
£Ø3£©ĻõĖįæÉŃõ»ÆŃĒĮņĖįøłĄė×Ó£¬°×É«³ĮµķAČō¼ÓŹŌ¼Į¢Ū¶ų²»¼ÓŹŌ¼Į¢Ś£¬¶ŌŹµŃéµÄÓ°ĻģŹĒ»įŹ¹SO32-¶ŌSO42-µÄ¼ģŃé²śÉśøÉČÅ£¬²»ÄÜČ·¶ØSO42-ŗĶSO32-ŹĒ·ń“ęŌŚ£¬
¹Ź“š°øĪŖ£ŗ»įŹ¹SO32-¶ŌSO42-µÄ¼ģŃé²śÉśøÉČÅ£¬²»ÄÜČ·¶ØSO42-ŗĶSO32-ŹĒ·ń“ęŌŚ£»
£Ø4£©ĘųĢåEĶØČėŹŌ¼Į¢Ü·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖSO2+Br2+2H2O=4H++SO42-+2Br-£¬
¹Ź“š°øĪŖ£ŗSO2+Br2+2H2O=4H++SO42-+2Br-£®
µćĘĄ ±¾Ģāæ¼²éĪŽ»śĪļµÄĶʶĻ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕĄė×ÓÖ®¼äµÄ·“Ó¦”¢ĻÖĻóĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėĶʶĻÄÜĮ¦µÄ漲飬עŅā°×É«³ĮµķµÄÅŠ¶Ļ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚ»Æѧ·“Ó¦¹ż³ĢÖŠ£¬·¢ÉśĪļÖŹ±ä»ÆµÄĶ¬Ź±²»Ņ»¶Ø·¢ÉśÄÜĮæ±ä»Æ | |
| B£® | ĻõĖįļ§ČÜÓŚĖ®ĪĀ¶Č½µµĶ£¬Õāøö¹ż³ĢĪüČČČČĮæ | |
| C£® | Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬H2ŗĶCl2ŌŚ¹āÕÕŗĶµćČ¼Ģõ¼žĻĀµÄ”÷H²»Ķ¬ | |
| D£® | ×Ō·¢·“Ó¦µÄģŲŅ»¶ØŌö“󣬷Ē×Ō·¢·“Ó¦µÄģŲŅ»¶Ø¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
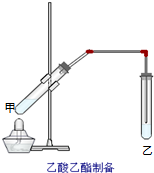 ČēĶ¼ŌŚŹŌ¹Ü¼×ÖŠĻČ¼ÓČė2mL 95%µÄŅŅ“¼£¬²¢ŌŚŅ”¶ÆĻĀ»ŗ»ŗ¼ÓČė2mLÅØĮņĖį£¬³ä·ÖŅ”ŌČ£¬ĄäČ“ŗóŌŁ¼ÓČė2æĖĪŽĖ®ŅŅĖį£¬ÓĆ²£Į§°ō³ä·Ö½Į°čŗó½«ŹŌ¹Ü¹Ģ¶ØŌŚĢś¼ÜĢØÉĻ£¬ŌŚŹŌ¹ÜŅŅÖŠ¼ÓČė5mL±„ŗĶµÄĢ¼ĖįÄĘČÜŅŗ£¬°“Ķ¼Į¬½ÓŗĆ×°ÖĆ£¬ÓĆ¾Ę¾«µĘ¶ŌŹŌ¹Ü¼×Š”»š¼ÓČČ3”«5minŗó£¬øÄÓĆ“ó»š¼ÓČČ£¬µ±¹Ū²ģµ½×óŹŌ¹ÜÖŠÓŠĆ÷ĻŌĻÖĻóŹ±Ķ£Ö¹ŹµŃ飮ŹŌ»Ų“š£ŗ
ČēĶ¼ŌŚŹŌ¹Ü¼×ÖŠĻČ¼ÓČė2mL 95%µÄŅŅ“¼£¬²¢ŌŚŅ”¶ÆĻĀ»ŗ»ŗ¼ÓČė2mLÅØĮņĖį£¬³ä·ÖŅ”ŌČ£¬ĄäČ“ŗóŌŁ¼ÓČė2æĖĪŽĖ®ŅŅĖį£¬ÓĆ²£Į§°ō³ä·Ö½Į°čŗó½«ŹŌ¹Ü¹Ģ¶ØŌŚĢś¼ÜĢØÉĻ£¬ŌŚŹŌ¹ÜŅŅÖŠ¼ÓČė5mL±„ŗĶµÄĢ¼ĖįÄĘČÜŅŗ£¬°“Ķ¼Į¬½ÓŗĆ×°ÖĆ£¬ÓĆ¾Ę¾«µĘ¶ŌŹŌ¹Ü¼×Š”»š¼ÓČČ3”«5minŗó£¬øÄÓĆ“ó»š¼ÓČČ£¬µ±¹Ū²ģµ½×óŹŌ¹ÜÖŠÓŠĆ÷ĻŌĻÖĻóŹ±Ķ£Ö¹ŹµŃ飮ŹŌ»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉśĪļÖŹÄÜĄ“ÉīÓŚÖ²Īļ¼°Ęä¼Ó¹¤²śĘ·ĖłÖü“ęµÄÄÜĮ棬ֱ½ÓČ¼ÉÕŹĒĄūÓĆ·½Ź½Ö®Ņ» | |
| B£® | ŹÆÓĶµÄĮŃ»ÆÓėĮŃ½ā¶¼ŹĒ»Æѧ±ä»Æ£¬¶ųĆŗµÄĘų»ÆÓėŅŗ»ÆŹĒĪļĄķ±ä»Æ | |
| C£® | ÓĆøßŃ¹ĒāĘų”¢ŃõĘųÖĘ×÷Č¼ĮĻµē³ŲŹĒĒāÄÜŌ“ĄūÓƵÄŅ»ÖÖÖŲŅŖ·½Ź½ | |
| D£® | »Æѧ·“Ó¦¹ż³ĢÖŠ·“Ó¦ĪļµÄ×ÜÄÜĮæŠ”ÓŚÉś³ÉĪļµÄ×ÜÄÜĮ棬ĶłĶł°éĖęČČĮæµÄĪüŹÕ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH4+”¢Fe3+”¢SO42-”¢Cl- | B£® | Mg2+”¢Ag+”¢CO32-”¢Cl- | ||
| C£® | K+”¢NH4+”¢SO42-”¢Cl- | D£® | K+”¢Na+”¢NO3-”¢HCO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÅäÖĘ450mLČÜŅŗŠčŅŖÓƵ½450mLČŻĮæĘæ | |
| B£® | ÓĆ¾Ę¾«ŻĶČ”µāĖ®ÖŠµÄµā | |
| C£® | ³ĘĮæNaOH ¹ĢĢåŹ±£¬½«NaOH ¹ĢĢå·ÅŌŚĶŠÅĢĢģĘ½×óÅĢµÄÖ½ÉĻ | |
| D£® | ÕōĮóŹ±£¬Ó¦½«ĪĀ¶Č¼ĘĖ®ŅųĒņææ½üÕōĮóÉÕĘæµÄÖ§¹ÜæŚ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
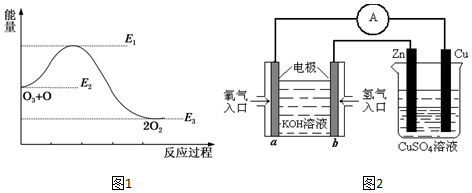
| A£® | v£ØC£©=0.2mol•L-1•s-1 | B£® | z=3 | ||
| C£® | BµÄ×Ŗ»ÆĀŹĪŖ25% | D£® | CĘ½ŗāŹ±µÄÅضČĪŖ0.5mol•L-1 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com