
【题目】运用基本公式进行计算:
(1)标准状况下,①4g氢气、 ②33.6L甲烷(CH4)、 ③6.02×1024个水分子、④1mol NH3中,
分子数由大到小的顺序为 ____________________(填序号,下同),含氢原子数最多的是_________,体积最大的是____________。
(2)现将200 mL 0.30 mol/L的盐酸与50 mL 0.80 mol/L CaCl2溶液混合(混合后体积变化忽略不计),
所得溶液中Cl-的物质的量浓度是_____________________。
(3)已知224L标准状况下的HCl气体完全溶于1L水(密度为1g/cm3)得到密度为1.1g/cm3的盐酸,此盐酸的物质的量浓度为:__________________ (保留一位小数)。
【答案】③>①>②>④③①0.56 mol/L8.1 mol/L
【解析】
(1)①氢气的物质的量为![]() =2mol,②标准状况下甲烷的物质的量为
=2mol,②标准状况下甲烷的物质的量为![]() =1.5mol,③水的物质的量为
=1.5mol,③水的物质的量为![]() =1mol,④NH3物质的量为1mol,显然物质的量越大分子数越大,则,分子数由大到小的顺序为③>①>②>④;含氢原子数分别为2mol×2×NAmol-1=4NA、1.5mol×4×NAmol-1=6NA、1mol×2×NAmol-1=2NA、1mol×3×NAmol-1=3NA,故含氢原子数最多的是③;相同状况下,物质的量越大,气体的体积越大,则体积最大的为①;
=1mol,④NH3物质的量为1mol,显然物质的量越大分子数越大,则,分子数由大到小的顺序为③>①>②>④;含氢原子数分别为2mol×2×NAmol-1=4NA、1.5mol×4×NAmol-1=6NA、1mol×2×NAmol-1=2NA、1mol×3×NAmol-1=3NA,故含氢原子数最多的是③;相同状况下,物质的量越大,气体的体积越大,则体积最大的为①;
(2)所得溶液中Cl-的物质的量为:0.2L×0.3mol/L+0.05L×0.8mol/L×2=0.14mol,所得溶液中Cl-的物质的量浓度是![]() =0.56mol/L;
=0.56mol/L;
(3)224L标准状况下的HCl气体物质的量为![]() ,完全溶于1L水(密度为1g/cm3)得到密度为1.1g/cm3的盐酸,所得溶液的体积为
,完全溶于1L水(密度为1g/cm3)得到密度为1.1g/cm3的盐酸,所得溶液的体积为![]() ,此盐酸的物质的量浓度为:
,此盐酸的物质的量浓度为:![]() 。
。


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
【题目】在一隔热系统中,初始温度为25℃,向20.00mL0.1000mol/L的氨水中逐滴加入0.1000mol/L的HC1溶液,测得混合溶液的温度变化如图所示。下列相关说法正确的是

A. 已知:25℃时,0.1000mol/L氨水的电离度为1.33%,该氨水的pH约为12
B. 若a点溶液呈碱性,则a点溶液中:c(NH4+)>c(Cl-)>c(NH3H2O)
C. b点溶液pH=7,c点溶液pH<7
D. b点溶液中: 0.1000mol/L +c(OH-)=c(Cl-)- c(NH3H2O)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于乙酸和乙醇的叙述正确的是
A.都能使石蕊溶液变红
B.分子中原子之间只存在单键
C.都能与钠反应并生成H2
D.都能与NaHCO3反应并生成CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关键能数据如表
化学键 | Si—O | O=O | Si—Si |
键能/kJ·mol-1 | x | 498.8 | 176 |
晶体硅在氧气中燃烧的热化学方程式:Si(s)+O2(g)=SiO2(s);ΔH=-989.2 kJ·mol-1,则表中x的值为 ( )
A.460B.920
C.1165.2D.423.3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)有关下列有机物的说法中错误的是
A. 石油经分馏后再通过裂化和裂解得到汽油
B. 植物油通过氢化加成可以变成脂肪
C. 用灼烧的方法可以区别蚕丝和合成纤维
D. 在做淀粉的水解实验时,用碘水检验淀粉是否完全水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)在2L定容密闭容器中通入1molN2(g)和3molH2(g),发生反应:
3H2(g)+N2(g)![]() 2NH3(g)△H<0,测得压强一时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。
2NH3(g)△H<0,测得压强一时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。

①若图中c=1.6mol,则改变的条件是__________(填字母,下同);
A.升温 B.降温 C.加压 D.减压 E.加催化剂
②若图中c<1.6mol,则改变的条件是__________(填字母);此时该反应的平衡常数__________(填“增大”、“减小”、“不变”)。
(2)如图甲,平衡时氢气的转化率为____________。
Ⅱ.粗制的CuCl2·2H2O晶体中常含有Fe3+、Fe2+杂质,为制得纯净的氯化铜晶体,首先将其制成水溶液,再按下图所示的操作步骤进行提纯。
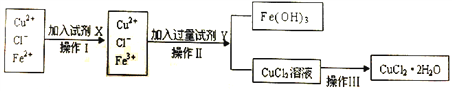
(1)操作Ⅰ时,常先加入合适的氧化剂,将Fe2+氧化为Fe3+,下列可选用的氧化剂是__________。
A.KMnO4 B.H2O2 C.Cl2 D.HNO3
(2)操作Ⅱ调整溶液的pH的Y试剂可选用下列中的__________。
A.NaOH(s) B.氨水 C.CuO(s) D.Cu(OH)2(s)
(3)已知溶度积常数如下表:
物质 | Cu(OH) | Fe(OH)2 | Fe(OH)3 |
Ksp | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
将溶液的pH调至pH=4时,使Fe3+完全转化为Fe(OH)3沉淀而除去,此时c(Fe3+)=__________。
(4)若将CuCl2溶液蒸干后,再灼烧,得到的固体是__________(填化学式);操作Ⅲ后由CuCl2·2H2O晶体得到纯净无水CuCl2的合理操作是_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X.Y、Z、W四种短周期元素,它们在周期表中位置如图所示,下列说法正确的是

A. 四种元素的原子半径由小到大的顺序为:r(X)<r(Z)<r(W)<r(Y)
B. X、Y、Z既能形成离子化合物,又能形成共价化合物
C. X与其余三种元素之间形成的核外电子总数为10的微粒只有2种
D. H2Z的熔点比HW高,是因为它们的晶体类型不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始反应后,反应速率最快和最慢的容器编号分别是
容器编号 | 温度 | SO2的物质的量 | O2的物质的量 | 催化剂 |
甲 | 500 ℃ | 10 mol | 5 mol | - |
乙 | 500 ℃ | 10 mol | 5 mol | V2O5 |
丙 | 500 ℃ | 8 mol | 5 mol | - |
丁 | 450 ℃ | 8 mol | 5 mol | - |
A.甲、乙B.甲、丙C.乙、丁D.丙、丁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com