
【题目】下列关于物质的元素组成或分类的说法正确的是
A.碱都含氢元素B.酸都含氧元素
C.盐都含金属元素D.漂粉精、液氯、干冰均为混合物
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】某实验小组利用右图所示装置制取氨气。请回答下列问题:

(1)实验室制备氨气的化学方程式是____________________________________________________。
(2)请指出装置中的两处错误
①____________________________;②____________________________。
(3)检验试管中收集满氨气的方法是___________________________________________________。
(4)用下列装置吸收多余的氨气,最合理的是_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
(1)高铁电池的负极材料是____。
(2)放电时,正极发生____(填“氧化”或“还原”)反应;已知负极反应为Zn-2e-+2OH-====Zn(OH)2,则正极反应为_______________________。
(3)放电时,____(填“正”或“负”)极附近溶液的碱性增强。
II、在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,回答下列问题:
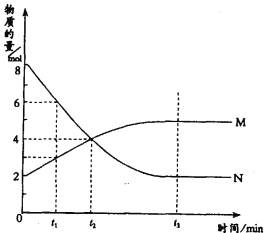
(4)反应的化学方程式为:______________。
(5)反应在_______时刻达到平衡状态。
(6)反应在_____时刻之前正反应速率大于逆反应速率。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为TS(中文名![]() ,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
A. TS是第七周期第ⅦA族元素 B. TS的同位素原子具有相同的电子数
C. TS在同族元素中非金属性最弱 D. 中子数为176的TS核素符号是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸是实验室及生活中的常见物质。
(1)写出醋酸的电离方程式______________。
(2)常温下醋酸溶液的pH <7,用文字描述其原因是____________。
(3)能证明醋酸是弱酸的实验事实是(多选、错选不得分)_________。
a.同浓度的CH3COOH溶液和盐酸分别与相同的Mg条反应,放出H2的初始速率醋酸慢
b.0.1 mol·L-1 CH3COONa溶液的pH> 7
c.CH3COOH溶液与Na2CO3反应生成CO2
d.0.1 mol·L-1 CH3COOH溶液可使紫色石蕊变红
e. 常温下0.1mol/l醋酸溶液的pH>1
(4)25 ℃时,在体积均为20 mL、浓度均为0.1 mol·L-1的CH3COOH、HCl溶液中,分别逐滴加入浓度为0.1 mol·L-1的NaOH溶液,溶液pH随加入NaOH溶液体积变化如图所示。
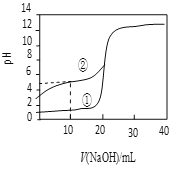
ⅰ.当加入NaOH溶液20 ml时,①溶液的离子浓度大小关系是____________ 。
ⅱ.当②溶液的pH=7时,溶液中存在的微粒浓度大小关系正确的是____________。
a.c(Na+)=c(Ac-)>c(HAc)>c(H+)=c(OH-)
b.c(Na+)=c(Ac-)>c(H+)=c(OH-)>c(HAc)
c.c(HAc)>c(Na+)=c(Ac-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是现代社会发展的支柱之一。
(1)化学反应中的能量变化,通常主要表现为热量的变化。
①下列反应中,属于放热反应的是___________(填序号)。
a. Ba(OH)2·8H2O与NH4Cl混合搅拌
b. 高温煅烧石灰石
c. 铝与盐酸反应
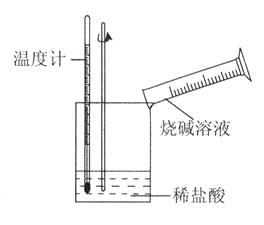
②某同学进行如下图所示实验,测量稀盐酸与烧碱溶液中和反应的能量变化。实验表明:反应温度升高,由此判断该反应是_______(填“吸热”或“放热”)反应,其离子方程式是_______________。
(2)电能是现代社会应用最广泛的能源之一。
下图所示的原电池装置中,其负极是_____________________,正极上能够观察到的现象是____________________________,正极的电极反应式是_________________________。
原电池工作一段时间后,若消耗锌6.5g,则放出气体__________g。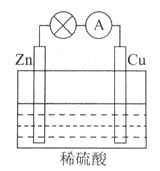
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列四个常用电化学装置的叙述正确的是( )
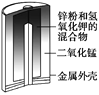
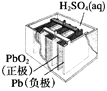
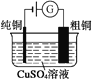
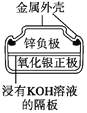
图1 碱性锌锰电池 图2 铅—硫酸蓄电池 图3 电解精炼铜 图4 银锌纽扣电池
A. 图1所示电池中,MnO2的作用是催化剂
B. 图2所示电池放电过程中,硫酸浓度不断增大
C. 图3所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图4所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示反应M(g)+P(g) ![]() nQ(g)的平衡体系中,Q的物质的量浓度c(Q)与温度T的关系(曲线上的点表示平衡状态)。下列有关该反应的描述错误的是( )
nQ(g)的平衡体系中,Q的物质的量浓度c(Q)与温度T的关系(曲线上的点表示平衡状态)。下列有关该反应的描述错误的是( )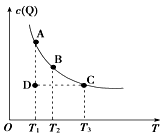
A.通过分析题图,该反应的正反应为放热反应
B.A状态与C状态的化学反应速率比较为v(A)<v(C)
C.在T1、D状态时,v正<v逆
D.在T2、B状态时,改变体积始终有v正=v逆 , 则n=2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)A、B、C为三种强电解质,它们在水中电离出的离子如下表所示:
阳离子 | Na+、K+、Cu2+ |
阴离子 | SO42-、OH- |
如图1所示装置中,甲、乙、丙三个烧杯中依次盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了32g。常温下各烧杯中溶液的pH与电解时间t的关系如图2所示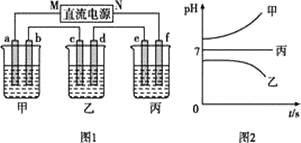
请回答下列问题:
(1)N为电源的(填“正”或“负”)极,电极b上发生的电极反应为。
(2)乙烧杯中的总反应为。
(3)计算电极e上生成的气体在标准状况下的体积为。
(4)丙烧杯要恢复到原来的状况,需要加入的物质和质量是。
(5)(Ⅱ)粗铜中一般含有锌、铁、银、金等杂质。在下图所示装置中,甲池的总反应方程式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O 接通电路一段时间后,精Cu电极质量增加了3.2g。在此过程中,甲池负极反应式 , 乙池硫酸铜溶液的浓度(填“变大”,“ 不变”,“变小”)。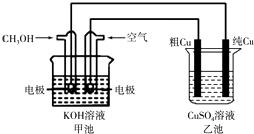
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com