
| A�� | ��H+��aq��+OH-��aq���TH2O��l����H=-57.3 kJ•mol-1����֪����0.5 mol H2SO4��Ũ��Һ�뺬1 mol NaOH����Һ��ϣ��ų���������57.3 kJ | |
| B�� | ��C��ʯī���TC�����ʯ����H=+1.19 kJ•mol-1����֪�����ʯ��ʯī���ȶ� | |
| C�� | ���������������������ֱ���ȫȼ�գ����߷ų��������� | |
| D�� | 2 g H2��ȫȼ������Һ̬ˮ�ų�285.8 kJ������������ȼ�յ��Ȼ�ѧ����ʽΪ��2H2��g��+O2��g���T2H2O��l����H=-285.8 kJ•mol-1 |
���� A��ǿ��ǿ��ϡ��Һ��ȫ��Ӧ����1molˮ�ų�������Ϊ��Ӧ���к��ȣ�Ũ�����ܽ���̷��ȣ�
B����������Խ��Խ���ã�
C���������仯Ϊ�������ȣ�
D��ȼ������1mol����ȼ�շų���������2g����Ϊ1mol����ȼ�յ��Ȼ�ѧ����ʽΪH2��g��+$\frac{1}{2}$O2��g��=H2O��l����H=-285.8 kJ•mol-1��
��� �⣺A��ǿ��ǿ��ϡ��Һ��ȫ��Ӧ����1molˮ�ų�������Ϊ��Ӧ���к��ȣ���0.5 mol H2SO4��Ũ��Һ�뺬1 mol NaOH����Һ��ϣ������ܽ���ȣ����Է�Ӧ�ų���������57.3 kJ����A��ȷ��
B����������Խ��Խ���ã���C��ʯī���TC�����ʯ����H=+1.19 kJ•mol-1����֪��ӦΪ���ȷ�Ӧ�����ʯ��������ʯī��ʯī�Ƚ��ʯ���ȶ�����B����
C���������仯Ϊ�������ȣ����������������������ֱ���ȫȼ�գ�ǰ�߷ų��������࣬��C����
D��ȼ������1mol����ȼ�շų���������2g����Ϊ1mol����ȼ�յ��Ȼ�ѧ����ʽΪH2��g��+$\frac{1}{2}$O2��g��=H2O��l����H=-285.8 kJ•mol-1����571.62H2��g��+O2��g���T2H2O��l����H=-571.6 kJ•mol-1����D����
��ѡA��
���� ���⿼�����Ȼ�ѧ����ʽ��д�������к��ȡ�ȼ���ȸ�������Ӧ�ã�ע����������Խ��Խ���ã����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��Ԫ�����ʻ��ã����ڶ�ĺ�������������Ԫ����-2�ۣ���Ҳ���γ�һ�������������۵Ļ����
��Ԫ�����ʻ��ã����ڶ�ĺ�������������Ԫ����-2�ۣ���Ҳ���γ�һ�������������۵Ļ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu��OH��2+HCl��Cu��OH��2+CH3COOH | B�� | NaHCO3+H2SO4��KHCO3+HCl | ||
| C�� | NaHCO3+NaOH��Ca��HCO3��2+NaOH | D�� | BaCl2+H2SO4��Ba��OH��2+H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ϊ292 | B�� | ������Ϊ116 | C�� | ������Ϊ292 | D�� | ������Ϊ176 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٣��ڣ��ۣ��ܣ��� | B�� | �ۣ��ܣ��ݣ��٣��� | C�� | �ݣ��ܣ��ۣ��ڣ��� | D�� | �ڣ��٣��ݣ��ܣ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �ϳ�
�ϳ� �������Լ��ͷ�Ӧ��������ȥ��
�������Լ��ͷ�Ӧ��������ȥ�� 
 ��D
��D

 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
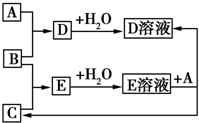 ��֪A��B��CΪ��ѧ��ѧ�г����ĵ��ʣ������£�AΪ���壬B��C��Ϊ���壮�����˵������£����ǿ�����ͼ���з�Ӧ������˵���в���ȷ���ǣ�������
��֪A��B��CΪ��ѧ��ѧ�г����ĵ��ʣ������£�AΪ���壬B��C��Ϊ���壮�����˵������£����ǿ�����ͼ���з�Ӧ������˵���в���ȷ���ǣ�������| A�� | A��B��C������Ԫ�ص���������Ԫ���γɵĻ��������������������������� | |
| B�� | A��B��C������Ԫ���γɵĻ����������������һ�����Ǽ� | |
| C�� | ���E��Һ��һ��ǿ�ᣬ��E��ҺΪ���� | |
| D�� | A��B��C����һ�ֽ�����ΪA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com