
【题目】下列物质既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
① Al2O3 ② Cu(OH)2 ③ Al(OH)3 ④ Na2CO3 ⑤ NaHCO3
A. ①②⑤ B. ②④ C. ①②④ D. ①③⑤
科目:高中化学 来源: 题型:
【题目】在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)![]() 2C(g) △H<0。t1 时刻达到平衡后,在t2 时刻改变某一条件,其反应过程如图所示。下列说法正确的是
2C(g) △H<0。t1 时刻达到平衡后,在t2 时刻改变某一条件,其反应过程如图所示。下列说法正确的是
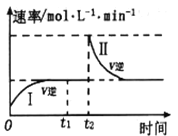
A. 0~t2时间段内,υ正> υ逆
B. I、Ⅱ两过程达到平衡时,A的体积分数I﹥II
C. t2时刻改变的条件可能是向密闭容器中加C
D. I、II两过程达到平衡时,平衡常数I﹤II
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中实验“操作和现象”与“结论”对应关系正确的一组是( )
操作和现象 | 结论 | |
A | 向纯碱中滴加足量浓盐酸,将产生的气体通入硅酸钠溶液,溶液变浑浊 | 酸性:盐酸>碳酸>硅酸 |
B | 取某溶液少量,加入盐酸酸化的氯化钡溶液, 出现白色沉淀 | 该溶液中一定含有大量 的SO |
C | 用铂丝蘸取少量某溶液进行焰色反应,呈黄色 | 该溶液一定是钠盐溶液 |
D | NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 | 结合H+的能力:CO |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ. (1)下列条件的改变能增大活化分子百分数的是_____________。
A.增大压强 B.增大反应物的浓度
C.升高温度 D.使用催化剂
(2)破坏(或形成)1 mol化学键所吸收(或放出)的能量称为键能。已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P-P 198、Cl-Cl 243、P-Cl 331。

则反应P4(s,白磷)+6Cl2(g)=4PCl3(s)的反应热△H=__________kJ·mol-1。
Ⅱ.2SO2(g)+O2(g)![]() 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。

已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99 kJ·mol-1。请回答下列问题:
(1)图中C表示___________,E表示______________;该反应通常用V2O5作催化剂,加V2O5会使图中B点降低,理由是____________ ;
(2)图中△H=_________kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对储氢材料CaH2描述错误的是( )
A.离子半径:H->Li+B.H-有强还原性
C.Ca2+最外层电子排布式:3s23p6D.CaH2晶体中既有离子键又有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向2l恒温恒容容器中加入2molMgSO4并充入 2molCO,发生反应:MgSO4(s)+ CO(g)![]() MgO(s)+ CO2(g)+SO2(g)△H > 0 。测得反应过程中残留固体的质量随时间变化如图所示,下列说法不正确的是
MgO(s)+ CO2(g)+SO2(g)△H > 0 。测得反应过程中残留固体的质量随时间变化如图所示,下列说法不正确的是
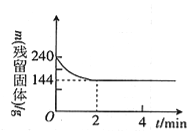
A. 0 ~2min内平均反应速率v(SO2)= 0.3 mol·l-1 ·min-1
B. 2 ~4min内容器内气体的密度没有变化
C. 该温度下,反应的平衡常数为1.8
D. 保持其他条件不变,起始时向容器中充入1.00 mol MgSO4和1.00 molCO,反应达到平衡时,n(CO2)> 0.60 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请结合下图回答问题: 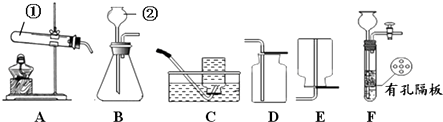
(1)写出有标号的仪器名称:① , ② .
(2)实验室用高锰酸钾制取O2的化学方程式为 , 用A、C装置制取O2时,为防止高锰酸钾进入导管,可采取的措施是 .
(3)实验室用B、D装置制取CO2的化学方程式为 , 若将发生装置由B改为F,其优点是 .
(4)SO2是无色有刺激性气味的有毒气体,密度比空气大,易溶于水.SO2的某些化学性质与CO2相似,实验中常用NaOH溶液吸收SO2尾气.用下图所示装置收集一瓶干燥的SO2 , 装置中导管按气流方向连接顺序是→⑤(填序号);图中漏斗的作用是;烧杯中NaOH溶液的作用是(用化学方程式表示). 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com