
 碳酸二甲酯(DMC)是一种近年来受到广泛关注的环保型绿色化工产品。在催化剂作用下,可由甲醇和CO2直接合成DMC:CO2 + 2CH3OH → CO(OCH3)2 + H2O,但甲醇转化率通常不会超过1%是制约该反应走向工业化的主要原因。某研究小组在其他条件不变的情况下,通过研究温度、反应时间、催化剂用量分别对转化数(TON)的影响来评价催化剂的催化效果。计算公式为:TON=转化的甲醇的物质的量/催化剂的物质的量。
碳酸二甲酯(DMC)是一种近年来受到广泛关注的环保型绿色化工产品。在催化剂作用下,可由甲醇和CO2直接合成DMC:CO2 + 2CH3OH → CO(OCH3)2 + H2O,但甲醇转化率通常不会超过1%是制约该反应走向工业化的主要原因。某研究小组在其他条件不变的情况下,通过研究温度、反应时间、催化剂用量分别对转化数(TON)的影响来评价催化剂的催化效果。计算公式为:TON=转化的甲醇的物质的量/催化剂的物质的量。
(1)已知25℃时,甲醇和DMC的标准燃烧热分别为△H1和△H2,则上述反应在25℃时的焓变△H3=___________。
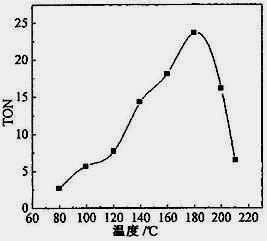
(2)根据反应温度对TON的影响图(下左图)判断该反应的焓变△H________0(填“>”、“=”或“<”),理由是________________________________。
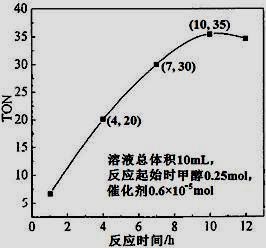
(3)根据反应时间对TON的影响图(上右图),已知溶液总体积10mL,反应起始时甲醇0.25mol,催化剂0.6×10—5 mol,计算该温度下,4~7 h内DMC的平均反应速率:________;计算10 h时,甲醇的转化率:________。
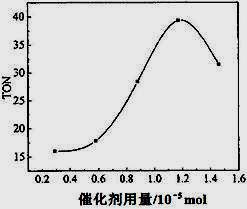
(4)根据该研究小组的实验及催化剂用量对TON的影响图(左图),判断下列说法正确的是___ __。
a. 由甲醇和CO2直接合成DMC,可以利用价廉易得的甲醇把影响环境的温室气体CO2转化为资源,在资源循环利用和环境保护方面都具有重要意义
b. 在反应体系中添加合适的脱水剂,将提高该反应的TON
c. 当催化剂用量低于1.2×10—5 mol时,随着催化剂用量的增加,甲醇的平衡转化率显著提高
d. 当催化剂用量高于1.2×10—5 mol时,随着催化剂用量的增加,DMC的产率反而急剧下降
科目:高中化学 来源: 题型:
我国湘黔渝三地交界地区是中国电解锰企业最集中的地区,被称为中国的“锰三角”。金属锰的熔点很高,常用铝热法制得粗锰,再用电解法制得纯的金属锰。铝被用于冶炼金属锰,是因为铝 ( )
A.熔点低
B.具有还原性
C.具有两性
D.冶炼反应中放出大量的热
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验方案不能达到实验目的的是( )
| 实验目的 | 实验方案 | |
| A | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液 |
| B | 证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 | 向2 mL 1 mol·L-1NaOH溶液中先加入3滴1 mol·L-1MgCl2溶液,再加入3滴 1 mol·L-1FeCl3溶液 |
| C | 检验蔗糖水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,然后加入足量稀NaOH溶液,再向其中加入新制的银氨溶液,并水浴加热 |
| D | 探究温度对化学平衡的影响 | 将NO2球浸泡在冷、热水中,观察颜色的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A(g)+B(g)  C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| 温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
请回答下列问题:
(1)该反应平衡常数表达式为K=________;ΔH________0(填“>”“<”或“=”)。
(2)830 ℃时,向一个5 L的密闭 容器中充入0.20 mol的A和0.80 mol的B,若测得反应初始至6 s内A的平衡反应速率v(A)=0.003 mol·L-1·s-1,则6 s时c(A)=________mol·L-1;C的物质的量为________mol。
(3)在与(2)相同的温度、容器及A、B配比下反应经一段时间后达到平衡,此时A的转化率为________;如果这时向该密闭容器中再充入1mol氩气,则平衡时A的转化率________(填“增大”“减小”或“不变”)。
(4)判断该反应是否达到平衡的依据为________(填正确选项的字母)。
A.压强不随时间改变
B.气体的密度不随时间改变
C.c(A)不随时间改变
D.单位时间里生成C和D的物质的量相等
(5)1 200 ℃时反应C(g)+D(g)  A(g)+B(g)的平衡常数的值为________。
A(g)+B(g)的平衡常数的值为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
LED系列产品是被看好的一类节能新产品, 下图是一种氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是 ( )
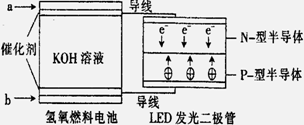
A.a处通入氢气,发生了还原反应: H2-2e-+2OH-=2H2O
B.b处通入氧气,为电池的正极
C.该装置中只涉及两种形式的能量转化,电池中的KOH溶液也可用稀硫酸溶液代替
D.P-型半导体连接的是电池负极
查看答案和解析>>
科目:高中化学 来源: 题型:
由CH3CH3→CH3CH2Cl→CH2=CH2→CH3CH2OH的转化过程中,经过的反应类型
是( )
A.取代反应→加成反应→氧化反应
B.裂解反应→取代反应→消去反应
C.取代反应→消去反应→加成反应
D.取代反应→消去反应→裂解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
工业合成UV高级油墨的主要成分的路线图如下:
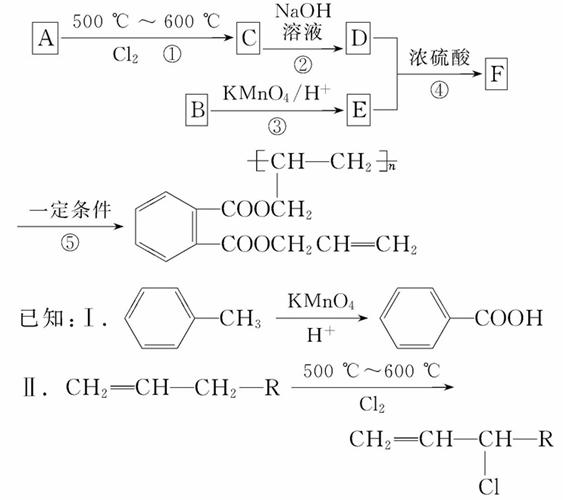
请回答:
(1)A的结构简式为___________________________________________。
(2)下列有关D的说法,正确的是_______(填序号)。
A.能使紫色石蕊试液变红
B.能发生缩聚反应
C.能发生取代反应
D.能发生加成反应
(3)F的官能团有_______种(不含苯环)。1 mol F与氢氧化钠溶液共热,最多能消耗_______mol NaOH。
(4)反应②的化学方程式为_______________________________________。
(5)E有多种同分异构体,写出同时符合以下条件的同分异构体的结构简式_______________________________________。
①与NaHCO3反应能生成CO2气体
②与新制氢氧化铜悬浊液共热能生成红色沉淀
③苯环上的一氯代物只有2种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
“绿色化学”的核心理念是:原子经济性原则。即力求反应物分子中的所有原子全都转化到目标产物中,理想状态的原子利用率为100%。在合成1,2—二溴乙烷时,原子利用率最高的途径是
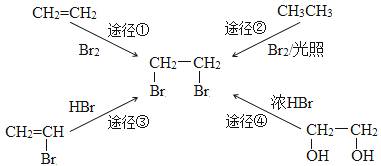
A.途径① B.途径② C.途径③ D.途径④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作正确且能达到预期目的的是( )
| 实验目的 | 操作 | |
| ① | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| ② | 欲证明CH2===CHCHO中含有碳碳双键 | 滴入KMnO4酸性溶液,看紫色是否褪去 |
| ③ | 欲除去苯中混有的苯酚 | 向混合液中加入浓溴水,充分反应后,过滤 |
| ④ | 证明SO2具有漂白性 | 将SO2通入酸性KMnO4溶液中 |
| ⑤ | 比较铜和镁的金属活动性强弱 | 用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液 |
| ⑥ | 比较碳和硅两元素非金属性强弱 | 测同温同浓度Na2CO3和Na2SiO2水溶液的pH |
A.①④⑤ B.②③⑤
C.①⑤⑥ D.①②③④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com