
| A. | 少量金属钠溶解在AlCl3溶液中:2Na+2H2O=2Na++H2↑ | |
| B. | 铝溶解在NaOH溶液中:2Al+2OH-+2H2O=2AlO2-+3H2↑ | |
| C. | MgO溶于醋酸中:MgO+2H+=H2O+Mg2+ | |
| D. | Al(OH)3溶于稀硫酸中:OH-+H+=H2O |
分析 A.钠与水反应生成氢氧化钠和氢气,少量的氢氧化钠与铝离子反应生成氢氧化铝沉淀;
B.铝与氢氧化钠溶液反应生成偏铝酸钠和氢气;
C.醋酸为弱酸,离子方程式中醋酸不能拆开;
D.氢氧化铝不能拆开,应该保留化学式.
解答 解:A.少量金属钠溶解在AlCl3溶液中,反应生成氢氧化铝沉淀、氢气和氯化钠,正确的离子方程式为:2Al3++6Na+2H2O=6Na++3H2↑+2Al(OH)3↓,故A错误;
B.铝溶解在NaOH溶液中,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,故B正确;
C.MgO溶于醋酸中,醋酸不能拆开,正确的离子方程式为:MgO+2CH3COOH=H2O+Mg2++2CH3COO-,故C错误;
D.氢氧化铝为难溶物,不能拆开,正确的离子方程式为:Al(OH)3+3H+=Al3++3H2O,故D错误;
故选B.
点评 本题考查了离子方程式的正误判断,题目难度中等,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.


科目:高中化学 来源: 题型:选择题
| A. | 该反应在40 min内的平均速率可表示为 ν(NH3)=0.001 mol/L•min | |
| B. | 该反应达到平衡时,保持其他条件不变,容器中NH3、N2、H2的物质的量保持相等 | |
| C. | 其他条件不变,升高温度,可使该反应的速率加快 | |
| D. | 达到平衡时,ν(NH3)=ν(N2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下2.24L己烷分子中含1.9NA对共用电子 | |
| B. | 常温下4.4g的CO2和N2O混合物中,所含有的原子数为0.3 NA | |
| C. | 0.1mol Fe与0.1 mol Cl2反应时失电子数为0.3NA | |
| D. | 电解精炼铜时,阳极质量每减少32g 电路中就转移NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
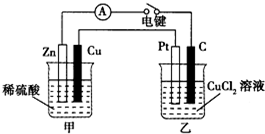 某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合装置的电键时,观察到电流表的指针发生了偏转.请回答下列问题:
某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合装置的电键时,观察到电流表的指针发生了偏转.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
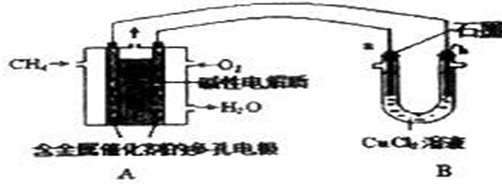
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学实验室中的蔗糖纯度很高,可用来食用 | |
| B. | 实验室中制取完有毒气体,开窗通风即可 | |
| C. | 为了节约用水,实验室中用过的废洗液,可以用来冲洗厕所 | |
| D. | 不能用手接触药品,不要把鼻孔凑到容器口去闻药品的气味,不得尝任何药品的味道 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com