
(1)下列每组分别给出了两个量,其中可以组成一个物质的量公式的组有(填编号)___________
① | ② | ③ | ④ | ⑤ |
物质所含的微粒数 | 固体体积 | 溶液的质量百分比浓度 | 标准状况下气体的摩尔体积 | 非标准状况下某物质的质量 |
阿伏加德罗常数 | 固体密度 | 溶液体积 | 标准状况下气体的体积 | 物质的摩尔质量 |
(2)在标准状况下:①6.72LCH4, ②3.01×1023个HCl分子, ③13.6gH2S, ④0.2molNH3,下列对这四种气体的描述正确的是(填写代号)___________
A.质量②>③>①>④ B.密度②>③>④>① C.体积②>③>①>④ D.氢原子数①>③>④>②
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题

 ;
; ;
; CH2CH2OOCH、
CH2CH2OOCH、 COOCH2CH3、
COOCH2CH3、 CH2COOCH3、
CH2COOCH3、 00CCH2CH3.
00CCH2CH3. CH(CH3)OOCH.
CH(CH3)OOCH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH=C(CH3)CH2CH3 | B. | (CH3)2C=CHCH2CH3 | ||
| C. | CH3CH=CHCH(CH3)2 | D. | CH2=CHCH2CH(CH3)2 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上10月月考化学试卷(解析版) 题型:选择题
光导纤维的主要成分是SiO2,下列关于SiO2的有关叙述正确的是
A.SiO2是酸性氧化物,它不溶于水也不溶于任何酸
B.SiO2是制造玻璃的主要原料之一,它在常 温下不与NaOH溶液反应
温下不与NaOH溶液反应
C.因高温时SiO2与Na2CO3反应放出CO2,所以H2SiO3酸性比H2CO3强
D.CO2通入水玻璃中可得硅酸
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上期中化学试卷(解析版) 题型:填空题
(1)写出反应用稀硫酸清洗铁锈(Fe2O3)的离子方程式:______________
(2)把离子反应Cu2++2OH-=Cu(OH)2↓ 改写成化学方程式______________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上期中化学试卷(解析版) 题型:选择题
卫生防疫人员要紧急配制0.01mol/L的KMnO4消毒液,下列操作导致所配溶液浓度偏高的是
A. 取KMnO4样品时不慎在表面沾了点蒸馏水
B. 溶解搅拌时有液体飞溅
C. 定容时俯视容量瓶刻度线
D. 摇匀后见液面下降,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上期中化学试卷(解析版) 题型:选择题
下列反应的离子方程式错误的是
A.铁与稀硫酸反应:Fe+2H +=Fe 2+ +H 2↑
B.碳酸氢钙与稀盐酸反应:Ca(HCO3)2 +2H+ =Ca2++2H2O+2CO2↑
C.盐酸跟氢氧化钾溶液反应:H++OH-=H2O
D.碳酸镁与硫酸反应:MgCO3 +2H + =Mg2++H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁沈阳东北育才学校高一阶段考一化学卷(解析版) 题型:推断题
含有A+、B3+ 、C3+ 三种金属阳离子的水溶液发生了如下一系列变化:
、C3+ 三种金属阳离子的水溶液发生了如下一系列变化:
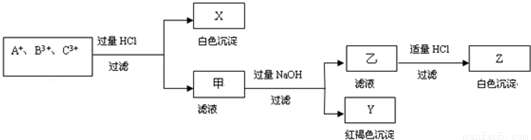
请通过分析回答(用化学符号填写):
(1)A+是______,B3+是____________,C3+是____________;
(2)X是____________,Y是____________,Z是____________;
(3)写出有关离子方程式:
①生成Y沉淀:_______________________;
②生成Z沉淀:_______________________.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com