
���� ��1����������һ�����ʵ���Ũ�ȵ���Һ�IJ����ǣ����㡢��ȡ��ϡ�͡���Һ��ϴ�ӡ����ݡ�ҡ����ѡ��ʹ�õ�������
�������������ʵ����ʵ�������Һ�����Ӱ�죬����C=$\frac{n}{V}$���з���������ʹnƫ�����ʹVƫС�IJ�������ʹ��ҺŨ��ƫ�ߣ���֮ʹ��ҺŨ��ƫ�ͣ�
��2����������ƿ���켰ʹ��ע��������
��� �⣺��1������һ�����ʵ���Ũ�ȵ���Һ�IJ����ǣ����㡢��ȡ��ϡ�͡���Һ��ϴ�ӡ����ݡ�ҡ�ȣ��õ�����������Ͳ���ձ�������������ͷ�ιܡ�100mL����ƿ��
�ٶ����Ǹ��ӿ̶��߹۲�Һ�棬������Һ���ƫС����ҺŨ��ƫ�ߣ���ѡ��
������ƿʹ��ʱδ��������ʵ����ʵ�������Һ������������Ӱ�죬�ʲ�ѡ��
�۶��ݺ���ҡ�ȡ����ã�����Һ����ڿ̶��ߣ��ټ�����ˮ�����̶ȣ�������Һ���ƫ�ߣ��ʲ�ѡ��
��ѡ���٣�
�ʴ�Ϊ��C E F��G��H���٣�
��2��A��ʹ������ƿǰ������Ƿ�©ˮ������������Һ��Ũ����������ȷ��
B������ƿ������ˮϴ�������ô�����Һϴ�ӣ��������ʵ����ʵ���ƫ��������Һ��Ũ��ƫ�ߣ��ʴ���
C������ƿΪ���������������ܽ���壬�ʴ���
D������ƿΪ������������������ϡ����Һ���ʴ���
E���Ǻ�ƿ�ǣ���ʳָ��סƿ��������һֻ�ֵ���ָ��סƿ�ף�������ƿ��ת��ҡ����Σ�Ŀ����ҡ����Һ������ȷ��
��ѡ��BCD��
���� ���⿼����һ�����ʵ���Ũ����Һ�����ƣ���ȷ����ԭ����ʵ����������ǽ���ؼ�����Ŀ�ѶȲ���ע�������������ͼ��ɣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��һ����KAl��SO4��2��Һ��һ����Ba��OH��2��Һ��ϣ�����������ǡ�����ʱ��Al3++2SO42-+3OH-+2Ba2+=2BaSO4��+Al��OH��3�� | |
| B�� | KMnO4��Ũ���ᷴӦ��Cl2��2MnO4-+16HCl=2Mn2++6Cl-+5Cl2��+8H2O | |
| C�� | 0.1molCl2��100mL1mol/LFeBr2��Ӧ��3Cl2+2Fe2++4Br-=6Cl-+2Fe3++2Br2 | |
| D�� | ��Al��OH��3�к����θ�Al��OH��3+3H+=Al3++3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 W��X��Y��Z�ֱ�ΪH��C��N��OԪ��
W��X��Y��Z�ֱ�ΪH��C��N��OԪ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
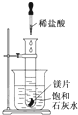 ��ͼ��ʾ����ʢ�м�С��þƬ���Թܷ���ʢ��25��ı���ʯ��ˮ���ձ��У����õι����Թ��е���2mL��ϡ���ᣮ���ж��ձ��е�ʵ�������������ԭ��˵������ȷ���ǣ�������
��ͼ��ʾ����ʢ�м�С��þƬ���Թܷ���ʢ��25��ı���ʯ��ˮ���ձ��У����õι����Թ��е���2mL��ϡ���ᣮ���ж��ձ��е�ʵ�������������ԭ��˵������ȷ���ǣ�������| A�� | �ձ��г��ְ�ɫ���ǣ�ԭ�����Թ��еķ�Ӧ�ų�����ʹ�ձ��б� ��ʯ��ˮ�¶����ߣ��������� | |
| B�� | �ձ��г��ְ�ɫ���ǣ�ԭ�����Թ��еķ�Ӧ��������ʹ�ձ��б���ʯ��ˮ�¶Ƚ��ͣ��������� | |
| C�� | �ձ���û���κ�����ԭ�����Թ��еķ�Ӧ���ձ��б���ʯ��ˮû�й�ϵ | |
| D�� | �ձ���û���κ�����ԭ�����Թ��еķ�Ӧ�Ȳ��ų�������Ҳ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH2Cl2+Br2$\stackrel{����}{��}$CHBrCl2+HBr | |
| B�� | CH3OH+HCl��CH3Cl+H2O | |
| C�� | CH3-CH2-Br+H2O$\stackrel{NaOH}{��}$CH3-CH2-OH+HBr | |
| D�� | 2Na+2H2O�T2NaOH+H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������Ӵ�С����1������100����֮�䣬�������ײ���ȫ�����ڽ��� | |
| B�� | CO2��ˮ��Һ�ܵ��磬����CO2Ϊ����� | |
| C�� | ��ʹ�ö����ЧӦ������FeCl3��Һ��Fe��OH��3���� | |
| D�� | 1 mol �κ����ʾ�����Լ6.02��1023��ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com