
 等物质的量的N2(g)和O2(g)在恒容密闭容器中反应:N2(g)+O2(g)?2NO(g),下图曲线a表示该反应在T℃时N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.下列叙述正确的是( )
等物质的量的N2(g)和O2(g)在恒容密闭容器中反应:N2(g)+O2(g)?2NO(g),下图曲线a表示该反应在T℃时N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.下列叙述正确的是( )| A. | T℃时,该反应的平衡常数K=$\frac{4({c}_{0}-{c}_{1})^{2}}{{{c}_{1}}^{2}}$ | |
| B. | T℃时,随着反应的进行,混合气体的密度减小 | |
| C. | 曲线b对应的条件改变可能是加入了催化剂 | |
| D. | 若曲线b对应的条件改变是温度,可判断该反应的△H<0 |
分析 A、依据氮气的浓度变化,找出三段式,计算平衡常数即可;
B、此容器为恒容密闭容器,ρ=$\frac{m}{V}$,据此判断即可;
C、催化剂只能改变化学反应速率,不能改变物质的转化率;
D、由图可知,b曲线化学反应速率快,若是升高温度,氮气的平衡浓度减小,则正反应为吸热反应.
解答 解:A、N2(g)+O2(g)?2NO(g),
起(mol/L) c0 c0 0
转(mol/L) c0 -c1 c0 -c1 2(c0 -c1 )
平(mol/L) c1 c1 2(c0 -c1 )
故K=$\frac{4({c}_{0}-{c}_{1})^{2}}{{{c}_{1}}^{2}}$,故A正确;
B、反应物和生成物均是气体,故气体的质量m不变,容器为恒容容器,故V不变,那么密度ρ=$\frac{m}{V}$不变,故B错误;
C、由图可知,b曲线氮气的平衡浓度减小,故应是平衡发生移动,催化剂只能改变速率,不能改变平衡,故b曲线不可能是由于催化剂影响的,故C错误;
D、由图可知,b曲线化学反应速率快(变化幅度大),氮气的平衡浓度减小,升高温度平衡正向移动,则正反应为吸热反应,即△H>0,故D错误,故选A.
点评 本题主要考查的是化学平衡建立的过程,涉及平衡常数的计算、平衡移动原理的应用、催化剂对平衡的影响等,综合性较强,有一定难度.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/LH2SO4与0.2mol/L 氨水各50mL | |
| B. | 0.1mol/LCH3COOH与0.1mol/LNaOH 溶液各50mL | |
| C. | pH=1的CH3COOH与pH=13的 NaOH 溶液各50mL | |
| D. | pH=1的盐酸与 pH=13的 NaOH 溶液各50mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 木材纤维和土豆淀粉遇碘水均显蓝色 | |
| B. | 食用花生油和鸡蛋清都能发生水解反应 | |
| C. | 包装用材料聚乙烯和聚氯乙烯都属于烃 | |
| D. | PX项目的主要产品对二甲苯属于饱和烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| t/min | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| n(Cl2)/10-3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅胶可用作食品干燥剂 | |
| B. | P2O5不可用作食品干燥剂 | |
| C. | 六水合氯化钙可用作食品干燥剂 | |
| D. | 加工后具有吸水性的植物纤维可用作食品干燥剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

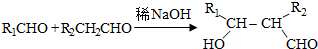
 .
. .
.
 (写结构简式)
(写结构简式)查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| Ca2+ | Mg2+ | Fe3+ | |
| 开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com