
某温度下,向一定体积0.1mol·L-1的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示则
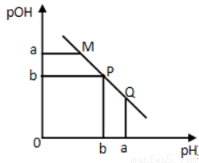
A.M点所示溶液的导电能力强于Q点
B.N点所示溶液中c(CH3COO-)>c(Na+)
C.M点和N点所示溶液中水的电离程度相同
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:高中化学 来源:2016-2017学年河南省高一上第一次考试化学卷(解析版) 题型:选择题
在标准状况下,将体积为V L的A气体,溶于100mL水中,得到密度为ρg•cm-3的溶液,A气体的摩尔质量为M g•mol-1,则此溶液的物质的量浓度为( )
A. B.
B.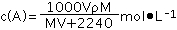
C. D.
D.
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上第12次周测化学卷(解析版) 题型:选择题
下列实验中,对应的现象及结论都正确且两者具有因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 在未知溶液中滴加BaCl2溶液出现白色沉淀,再加稀硝酸 | 沉淀不溶解 | 该未知溶液存在SO42-或SO32- |
B | 向稀的苯酚水溶液中滴加少量溴水 | 先看到白色沉淀,后消失 | 生成的三溴苯酚又重新溶于苯酚溶液中 |
C | 向某溶液中加入几滴新制的氯水,再向溶液中加入2滴KSCN溶液 | 溶液变为红色 | 该溶液中一定含有Fe2+ |
D | 在相同温度下,向1mL0.2mol·L-1NaOH溶液中滴入2滴0.1mol·L-1MgCl2溶液,再滴加2滴0.1mol·L-1FeCl3溶液 | 先产生白色沉淀,后生成红褐色沉淀 | Ksp[Mg(OH)2]>Ksp[Mg(OH)3] |
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上10月月考化学试卷(解析版) 题型:选择题
气体X可能由NH3、Cl2、HBr、CO2中的一种或几种组成,已知X通入AgNO3溶液时产生浅黄色沉淀,该沉淀不溶于稀HNO3,若将X通入澄清石灰水中,无沉淀产生,则有关气体X的成分的下列说法正确的是( )
①一定含有HBr,可能含有CO2 ②一定不含CO2
③一定不含NH3、Cl2 ④可能含有Cl2、CO2.
A.只有① B.只有③ C.①和③ D.②和③
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上10月月考化学试卷(解析版) 题型:选择题
化学与材料、能源、环境等密切联系。下列说法不正确的是( )
A.研发光电转换材料,充分利用太阳能
B.包装材料聚氯乙烯属于烃,会造成环境污染
C.用石灰对煤燃烧形成的烟气脱硫,并回收石膏
D.研发高效生物生长调节剂,减少对化肥的使用
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上10.6周测化学试卷(解析版) 题型:选择题
已知常温下CH3COOH和NH3·H2O的电离常数相等,向10ml浓度为0.1mol/L的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中
A.水的电离程度始终增大
B.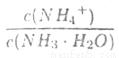 先增大再减小
先增大再减小
C.c(CH3COOH)与c(CH3COO-)之和始终保持不变
D.当加入氨水的体积为10mL时c(NH4+)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上10.6周测化学试卷(解析版) 题型:选择题
下列判断正确的是
A.同温下,HF比HClO易电离,则NaF溶液的pH比NaClO溶液的pH大
B.常温下,0.4mol·L-1溶液和0.2mol·L-1NaOH溶液等体积混合后的pH等于3,则混合溶液中离子浓度大小关系:c(A-)>c(Na+)>c(HA)>c(H+)>c(OH-)
C.常温下,BaSO4在饱和Na2SO4溶液中的Ksp比在纯水中的Ksp小
D.用铂电极电解食盐水,一段时间后两极产生气体体积比为3:2(同条件下),为将电解液恢复原状,则只需向电解液中通入一定量的HCl气体
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上学期第一次月考化学卷(解析版) 题型:填空题
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
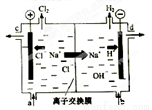
完成下列填空:
(1).写出电解饱和食盐水的离子方程式 。
(2).离子交换膜的作用为: 、 。
(3).精制饱和食盐水从图中 位置补充,氢氧化钠溶液从图中 位置流出。(选填“a”、“b”、“c”或“d”)
(4).KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂 ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式 。
ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月月考化学卷(解析版) 题型:选择题
利用催化技术可将汽车尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO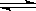 2CO2+ N2。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
2CO2+ N2。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO) /×10-3 mol·L-1 | 1.00 | 0.45 | 0.25 | 0.15 | 0.10 | 0.10 |
c(CO) / ×10-3 mol·L-1 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |


 下列说法中,不正确的是
下列说法中,不正确的是
 A.2s内的平均反应速率υ(N2)=1.875×10-4 mol·L-1·s-1
A.2s内的平均反应速率υ(N2)=1.875×10-4 mol·L-1·s-1
 B.在该温度下,反应的平衡常数K=5
B.在该温度下,反应的平衡常数K=5
 C.若将容积缩小为原来的一半,NO转化率大于90%
C.若将容积缩小为原来的一半,NO转化率大于90%
 D.使用催化剂可以通过提高活化分子百分数提高单位时间CO和NO的处理量
D.使用催化剂可以通过提高活化分子百分数提高单位时间CO和NO的处理量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com