
已知在常用催化剂(如铂、钯)的催化下,氢气和炔烃加成生成烷烃,难于得到烯烃,但使用活性较低的林德拉催化剂[Pd/(PdO、CaCO3),其中钯附于碳酸钙及少量氧化铅上],可使炔烃的氢化停留在生成烯烃的阶段,而不再进一步氢化。现有一课外活动兴趣小组利用上述设计了一套由如下图所示仪器组装而成的实验装置(铁架台未画出),拟由乙炔制得乙烯,并测定乙炔氢化的转化率。若用含0.020molCaC2的电石和1.60g含杂质18.7%的锌粒(杂质不与酸反应)分别与足量的X和稀硫酸反应,当反应完全后,假定在标准状况下测得G中收集到的水VmL。试回答有关问题。
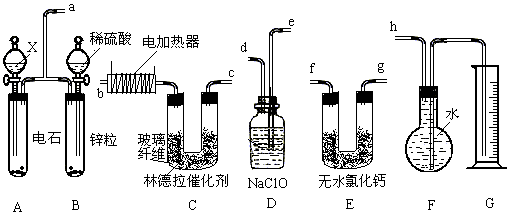
(1)所用装置的连接顺序是 (填各接口的字母)。
(2)写出A、C中所发生的两个反应的化学方程式(有机物写结构简式):
A
C
(3)为减慢A中的反应速率,X应选用_________________,操作时还应采取的措施是_________________________________________________。
(4)F中留下的气体除含少许空气外,还有______________________。G所选用的量筒的容积较合理的是_______。
(A)500mL (B)1000mL (C)2000mL
(5)若V=672mL(导管内气体体积忽略不计),则乙炔氢化的转化率为_______________。
【答案】(1)a、e、d、f、g、b、c、h(f、g可调换);
(2)A: (2分)
(2分)
C: (2分)
(2分)
(3)饱和食盐水(1分)通过调节分液漏斗活塞,降低食盐水的滴速(2分)
(4)H2、C2H4、C2H2(2分) B(2分)
50%
【解析】
(1)先产生乙炔和氢气,除杂,反应,测量。
(2)A 电石和水生成乙炔和氢氧化钙。
C 乙炔和氢气的催化加氢。
(3)电石和水的反应较剧烈,用饱和食盐水来代替水。操作时可以通过调节分液漏斗活塞,降低食盐水的滴速。
(4)F中留下的气体除含少许空气外,还有没有反应的氢气,乙炔和没有吸收的乙烯。
1.60g含杂质18.7%的锌粒的摩尔数为: (1.60x81.3%)/65.4=0.0199(以0.02算),而CaC2也为0.02,按等摩尔计算。 1mol理想气体的体积为22.4升。0.02mol为: 0.02x22.4=0.448升=448毫升
由于乙炔本身的产量根据0.02mol计算为约450毫升。从0.02mol锌加酸产生的氢气也是约450毫升。当乙炔和氢气完全不反应的时候(比如催化剂失效了),两个体积是相加的关系:450+450=900ml。只有当完全反应时最终产物体积才为450ml。由于大部分有机反应均为不完全反应,所以很有可能最终体积在450ml与=900ml之间。所以用1000ml最合适。而500ml太小。
(5)
0.02mol乙炔反应的0.02mol乙烯。V=0.02*22.4=0.448L=448Ml,现在体积大于计算的体积,则说明没有转化完全。多余的V=672-448=224Ml
假设转化的乙炔为x,则
初始 0.02 0.02 0
反应 x x x
余下 0.02-x 0.02-x x
[2(0.02-x)+x]*22400=672
X=0.01
乙炔氢化的转化率=0.01/0.02*100%=50%。


科目:高中化学 来源: 题型:
离子化合物:将化学式中离子的电子式按连接顺序写在一起即可。如:
MgCl2 ____________________
NaOH ____________________
NH4Cl ____________________
Na2O2 ________________ ____
____
查看答案和解析>>
科目:高中化学 来源: 题型:
有甲、乙、丙三种试液,在氢氧化钡溶液中加入甲,有白色沉淀生成,在沉淀中加入乙,沉淀完全溶解,并有气泡生成,最后向所得溶液中加入丙又产生白色沉淀,则甲、乙、丙依次是 ( )
A.K2CO3、HCl、CaCl2 B.Na2CO3、HNO3、MgCl2
C.Na2CO3、HCl、AgNO3 D.H2SO4、Na2CO3、AgNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
某烃的分子式为C10H14,不能使溴水褪色,但可使酸性KMnO4溶液褪色,分子结构中只含一个烷基,则此烷基的结构有( )
A. 2种 B. 3种 C. 4种 D. 5种
查看答案和解析>>
科目:高中化学 来源: 题型:
已知乙炔(C2H2)、苯(C6H6)、乙醛(C2H4O)的混合气体中含氧元素的质量分数为8%,则混合气体中碳元素的质量分数为( )
A.84% B.60% C.91% D.42%
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示:

(1)D的化学式是____________,E的化学式是________。
(2)A和B反应生成C的化学方程式是________________________________________
________________ ________________________________________________________。
________________________________________________________。
(3)E和F反应生成D、H和G的化学方程式是_________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y、Z为三种主族元素,可分别形成Xn+、Ym+、Zn-三种离子,已知m>n且X、Y、Z三种原子的M层电子数均为奇数。下列说法中不正 确的是 ( )
确的是 ( )
A.三种离子中,Ym+的离子半径最小
B.Z的最高价氧化物对应水化物的分子式为HnZO4
C.X、Y、Z一定在同一周期,且原子半径Z>X>Y
D.三种元素相应的最高价氧化物对应水化物之间两两会发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
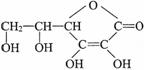 维生素C是一种重要的维生素,能防治坏血病,又称为抗坏血酸,其结构简式如右图,下列有关它的叙述错误的是
维生素C是一种重要的维生素,能防治坏血病,又称为抗坏血酸,其结构简式如右图,下列有关它的叙述错误的是
A.它的分子式为C6H8O6
B.滴入淀粉和碘水的混合溶液,蓝色褪去,表现出还原性
C.它是一种水溶性维生素,高温易分解
D.在碱性溶液中能稳定地存在
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E五种元素,它们原子的核电荷数依次递增且均小于18。A元素原子核外只有1个电子;C是地壳中含量最多的元素;B、C可形成两种化合物BC和BC2,B的最高正价与最低负价绝对值相等,BC有毒,BC2可用于灭火;D元素的最外层电子数是其电子层数的三分之一;E—具有与Ar原子相同的电子层结构。
(1)写出A、C两种元素的符号:A , C 。
(2)写出D原子和E—离子的结构示意图:D原子 ,E—离子 。
(3)由A、B、C、D四种元素组成的常见化合物的化学式为 ,
其电离方程式为 。
(4)写出A、C、D三种元素组成的常见化合物的稀溶液,常温下和E的单质反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com