
| A. | C2H6 | B. | C2H4O2 | C. | C2H6O | D. | C2H4Cl2 |
分析 分子式只能表示一种物质,就是说它不存在同分异构体.同分异构体是分子式相同,但结构不同的化合物,根据是否存在同分异构体判断正误.
解答 解:A、C2H6为烷烃,不存在同分异构体,表示一种物质,故A正确;
B、C2H4O2 可以是乙酸、甲酸甲酯等物质,存在同分异构体,所以不能表示一种物质,故B错误;
C、C2H6O可以存在同分异构体,可以是CH3CH2OH,CH3OCH3,所以不能只表示一种物质,故C错误;
D、C2H4Cl2有1,1-二氯乙烷和1,2-二氯乙烷两种同分异构体,故D错误.
故选A.
点评 本题以纯净物为载体考查了同分异构现象,难度不大,注意纯净物必须是由同一种物质组成.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:计算题
| 项目名称 | 数据 | 参考值 |
| 尿素氮 | 3.95 | 2.00-6.10 m mol•L-1 |
| 葡萄糖 | 4.50 | 3.89-6.11 m mol•L-1 |
| 总胆固醇 | 3.80 | <5.20 m mol•L-1 |
| 甘油三酯 | 1.85↑ | <1.70 m mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,测定0.1mol•L-1CH3COOH的pH值,若pH大于1,即可证明为弱电解质 | |
| B. | 等体积的0.1mol•L-1HCl和0.1mol•L-1醋酸溶液,分别与等量的相同颗粒度的Zn反应,观察产生气泡的速率,即可证明 | |
| C. | 等体积的0.1mol•L-1HCl和 0.1mol•L-1醋酸溶液,比较中和这两种酸所需相同物质的量浓度的NaOH溶液的体积,即可证明 | |
| D. | 常温下,测一定浓度的CH3COONa溶液的pH值,若pH大于7,即可证明 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
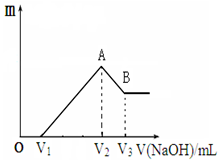 将镁、铝的混合物共0.1mol,溶于200mL 2.5mol•L-1的盐酸溶液中,然后再滴加2mol•L-1的NaOH溶液.请回答下列问题:
将镁、铝的混合物共0.1mol,溶于200mL 2.5mol•L-1的盐酸溶液中,然后再滴加2mol•L-1的NaOH溶液.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
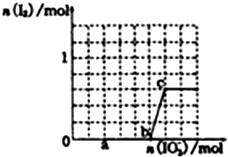 (1)铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
(1)铁及其化合物在生活、生产中有广泛应用.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | a表示有催化剂,b表示无催化剂 | B. | 若其他条件相同,a比b的温度高 | ||
| C. | 反应由逆反应开始 | D. | a→b采用的是加压 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com