
| 试验编号 | c(S2O82-)/mol•L-1 | c(Cr3+)/mol•L-1 | c(Ag+)/mol•L-1 | 时间/min |
| ① | 0.10 | 10.0 | 5.0 | 10 |
| ② | 0.10 | 10.0 | 2.5 | 20 |
| ③ | 0.20 | 10.0 | 5.0 | 5 |
| ④ | 0.10 | 5.0 | 5.0 | 5 |
| A. | 增大c(Ag+),v(Cr3+)增大 | |
| B. | 实验②的v(Cr3+)为0.25mmol•L-1•min-1 | |
| C. | 增大c(S2O82-),v(Cr3+)增大 | |
| D. | 增大c(Ag+),v(Cr3+)不变 |
分析 影响化学反应速率的因素有浓度、温度、压强以及催化剂等因素,一般情况下在其它条件相同时,反应物的浓度越大,反应速率越快,本题中比较①③数据可以判断出,增大c(S2O82-),v(Cr3+)增大,对比①②组数据,可以判断出增大c(Ag+),v(Cr3+)增大,据此分析解答.
解答 解:A、对比①②组数据,可以判断出增大c(Ag+),v(Cr3+)增大,故A正确;
B、实验②的v(Cr3+)=$\frac{△c}{△t}$=$\frac{5mol/L}{20min}$=0.25mmol•L-1•min-1,故B正确;
C、比较①③数据可以判断出,增大c(S2O82-),v(Cr3+)增大,故C正确;
D、对比①②组数据,可以判断出增大c(Ag+),v(Cr3+)增大,故D错误;
故选D.
点评 本题考查化学反应速率及其影响因素,做题时注意对比表中的数据进行分析,不难得出结论.


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:选择题
| A. | ①③⑥ | B. | ①②④ | C. | ①②⑤ | D. | ③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,化合物  的名称为2,4-二乙基-丙基辛烷 的名称为2,4-二乙基-丙基辛烷 | |
| B. | 若两种二肽互为同分异构体,则二者的水解产物一定不相同 | |
| C. | 分子式为C5H5O2Cl并能与饱和NaHCO3溶液反应产生气体的有机物有(不含立体结构)有15种 | |
| D. | 某有机物的结构简式是  ,该有机物能够发生加成反应、取代反应、缩聚反应和消去反应 ,该有机物能够发生加成反应、取代反应、缩聚反应和消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
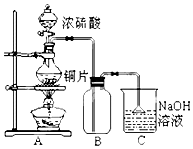 某研究性学习小组的同学为验证浓硫酸与铜能反应而稀硫酸不能,设计了如图所示装置进行探究:将6.4g 铜片和含0.2moL溶质的18.4mol/L浓硫酸放在圆底烧瓶中共热,直到无气体生成为止.(假定在此过程溶液体积不变)
某研究性学习小组的同学为验证浓硫酸与铜能反应而稀硫酸不能,设计了如图所示装置进行探究:将6.4g 铜片和含0.2moL溶质的18.4mol/L浓硫酸放在圆底烧瓶中共热,直到无气体生成为止.(假定在此过程溶液体积不变)| 序号 | 不合理的原因 | 误差 (偏低或偏高) | 改变措施 |
| 方案① | |||
| 方案② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | C2H4 | C. | C3H6 | D. | C4H10 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氯乙烯分子的结构简式:H3C-CH2Cl | B. | 硫原子的结构示意图: | ||
| C. | 过氧化钠的电子式: | D. | 中子数为10的氧原子:${\;}_{8}^{18}$O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:HClO4>HBrO4>HIO4 | B. | 还原性:Na+>S2->Br->Cl- | ||
| C. | 热稳定性:PH3>H2S>HCl>HF | D. | 水溶液酸性:HF>HCl>HBr>HI |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com