
| A. | 依据丁达尔现象可将分散系分为溶液、胶体与浊液 | |
| B. | 直径介于1-100nm之间的微粒称为胶体 | |
| C. | 胶体粒子很小,可以透过半透膜 | |
| D. | 鸡蛋清和豆浆都属于胶体 |
分析 A.分散系的划分是以分散质颗粒大小来区分的;
B.分散质粒度介于1nm~100nm之间的分散系属于胶体;
C.胶体粒子不能透过半透膜;
D.鸡蛋清和豆浆分散质都介于1nm~100nm之间.
解答 解:A.分散系的划分是以分散质颗粒大小来区分的,胶体粒子直径介于1nm~100nm之间,溶液溶质粒子直径小于1nm,浊液粒子直径大于100nm,溶液和浊液都不具有丁达尔效应,故A错误;
B.分散质直径介于1-100nm之间的分散系,称为胶体,故B错误;
C.胶体粒子不能透过半透膜,故C错误;
D.鸡蛋清和豆浆分散质都介于1nm~100nm之间,都是胶体,故D正确;
故选:D.
点评 本题考查了胶体的性质,明确分散系分类依据,熟悉胶体的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:实验题
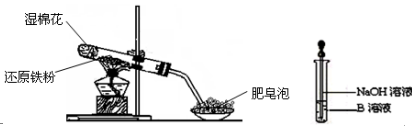
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
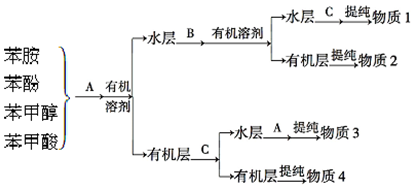
 )具有碱性.
)具有碱性.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | O |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑫ | ⑬ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 停止冬季供暖,减少有害物质排放 | |
| B. | 对锅炉和汽车等产生的有害气体和烟尘进行处理 | |
| C. | 退耕还林,改善生态环境 | |
| D. | 寻找新能源,减少化石燃料的使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
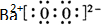 (写电子式).
(写电子式).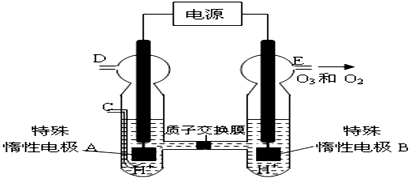
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C5H11CI的有机物,分子结构中含2个甲基的同分异构体有4种 | |
| B. | CH3COOH与C2H518OH在浓硫酸作用下加热,反应生有机物分子的结构简式为CH3COOC2H5 | |
| C. | 三氯甲烷只有一种结构,不存在同分异构,证明甲烷是正四面体构型 | |
| D. | 煎炸食物的花生油和牛油都是可皂化的饱和醋类 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com