


分析 (1)根据化学平衡常数K=$\frac{c(C{r}_{2}{{O}_{7}}^{2-})}{{c}^{2}(Cr{{O}_{4}}^{2-}){c}^{2}({H}^{+})}$进行计算;
(2)根据二氧化硫具有还原性,在酸性溶液中通SO2将Cr2O72-还原生成硫酸根和三价铬离子;根据Ksp[Cr(OH)3]=10-32计算c(OH-),从而计算PH;
(3)Fe作阳极失电子生成亚铁离子,提供还原剂;
(4)Cr(OH)3溶于稀硫酸生成硫酸铬和水,根据反应的量画出生成沉淀的物质的量与加入NaOH溶液体积的关系图.
解答 解:(1)若常温下pH=1溶液中Cr2O72-浓度为0.1mol•L-1,Cr2O72-浓度是CrO42-浓度的10倍即CrO42-浓度为0.01mol•L-1,化学平衡常数K=$\frac{c(C{r}_{2}{{O}_{7}}^{2-})}{{c}^{2}(Cr{{O}_{4}}^{2-}){c}^{2}({H}^{+})}$=$\frac{0.1}{0.0{1}^{2}×0.{1}^{2}}$=1.0×105,
故答案为:1.0×105;
(2)因为二氧化硫具有还原性,在酸性溶液中通SO2将Cr2O72-还原生成硫酸根和三价铬离子,所以离子方程式为:3SO2+Cr2O72-+2H+=2Cr3++3SO42-+H2O;因为Ksp[Cr(OH)3]=10-32,所以c(OH-)=$\root{3}{\frac{1{0}^{-32}}{1{0}^{-5}}}$=10-9mol•L-1,则PH=5,
故答案为:3SO2+Cr2O72-+2H+=2Cr3++3SO42-+H2O;5;
(3)电解还原法是利用电解产生的Fe2+将Cr2O72-还原为Cr3+,Fe作阳极失电子生成亚铁离子,提供Fe2+作还原剂,所以Fe与正极相连;
故答案为:正;
(4)Cr(OH)3溶于稀硫酸生成硫酸铬和水,化学方程式为2Cr(OH)3+3H2SO4=2Cr2(SO4)3+6H2O,往100.00mL 0.1000mol•L-1CrCl3溶液滴加1.000mol•L-1NaOH溶液,根据反应Cr3++3OH-=Cr(OH)3,Cr(OH)3+OH-=CrO2-+2H2O,所以应该为三份沉淀,一份溶解,生成沉淀的物质的量与加入NaOH溶液体积的关系图为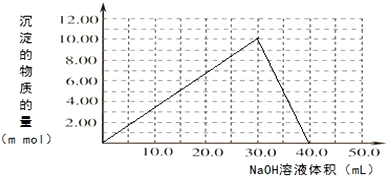 ,
,
故答案为:2Cr(OH)3+3H2SO4=2Cr2(SO4)3+6H2O; .
.
点评 本题考查了平衡常数的计算、氧化还原反应、溶度积常数的计算等知识点,题目难度中等,注意把握平衡常数和溶度积常数的表达式以及计算方法,侧重于考查学生的分析能力和计算能力.


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源: 题型:选择题
| A. | B的单质在自然界只有一种核素 | |
| B. | 元素C、D、E的简单离子的半径依次减小 | |
| C. | A、E分别与C形成的化合物中含有一种相同类型的化学键 | |
| D. | 这几种元素可能形成的简单离子中E的简单离子的还原性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
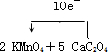
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
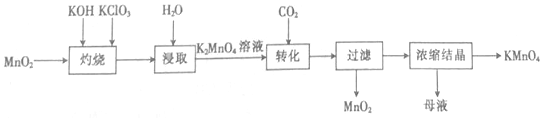
| A. | “灼烧”时,可在玻璃坩埚中进行 | |
| B. | “浸取”时,可用无水乙醇代替水 | |
| C. | “转化”反应中,氧化产物与还原产物的物质的量之比为2:1 | |
| D. | “浓缩结晶”后的母液中只有KMnO4和K2CO3两种溶质 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②向新制得的Na2S溶液中满加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体. |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉锭. |
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2具有氧化性,可用于漂白纸浆 | |
| B. | 医用消毒酒精中乙醇的浓度为95% | |
| C. | 用灼烧的方法可以区分蚕丝和人造纤维 | |
| D. | 硅胶作袋装食品的干燥剂时发生了化学变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com