单质碘有非常重要的用途,它的制备一般有两种方法:
方法一:海带、海藻燃烧后所得的灰份中含I
-,从中获得I
-,由 I
- 制备 I
2.
某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:
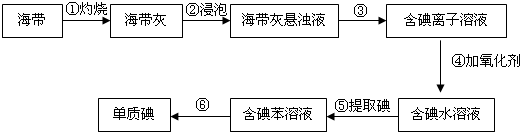
请回答:
(1)步骤①中灼烧海带用到的实验仪器有坩埚钳、铁三脚架、泥三角、酒精灯和
(填字母).
A.试管 B.瓷坩埚 C. 烧杯 D. 量筒
(2)步骤③的实验操作名称是
;
(3)步骤④中氧化剂最好选用
(填字母)
A.浓硫酸 B.新制氯水
C.酸性KMnO
4溶液 D.3%H
2O
2溶液和稀H
2SO
4混合液
其反应的离子方程式是
.
(4)步骤⑤中,学生选择用苯来提取碘,还可以用下列
(填字母)来提取碘.
A.乙酸 B.四氯化碳 C.酒精 D.己烷
(5)步骤⑤中,为了检验提取碘后的水溶液中是否还含有单质碘,取少量上述溶液于试管中,滴加
,如果看到
,则证明溶液中还含有碘.
(6)步骤⑤中为了得到含碘苯溶液,某学生设计了以下操作步骤:
a.将含碘的水溶液置于分液漏斗中
b.加入适量的苯
c.分离出下层液体
d.分离出上层液体,即得到含碘苯溶液
以上设计中有遗漏的操作.应该在步骤
(填字母)后,增加操作:
.
方法二:从智利硝石中获得碘酸钠(NaIO
3),再用NaHSO
3把碘酸钠还原为I
2.实际生产中分两步进行:
第一步:先用适量的 NaHSO
3将碘酸钠还原成I
-,反应的离子方程式为:
IO
3-+3HSO
3-=I
-+3SO
42-+3H
+;
第二步:向所得的酸性I
-溶液中加入适量的碘酸钠(NaIO
3)溶液便有碘析出,反应的离子方程式为
.




