
����Ŀ������������;������ȡ������������ͭ��
��ͭ��ϡ���ᷴӦ��
��ͭ��Ũ���ᷴӦ��
��ͭ����������Ӧ��������ͭ������ͭ�ٸ����ᷴӦ��������������ȷ����
A. ����;��������ͭ���������
B. ����;����������������ʵ�������>��>��
C. ;�������Ʊ��������������ɫ��ѧ������
D. ;�����б�������ͭ�뱻��ԭ����������ʵ���֮����3��2
���𰸡�B
�������������������ȡ����ͭ���йط�Ӧ��ͭ��ϡ���ᷴӦ��![]() ����ͭ��Ũ���ᷴӦ��Cu+4HNO3(Ũ)=Cu��NO3��2+2NO2��+2H2O����ͭ����������Ӧ��������ͭ������ͭ�ٸ����ᷴӦ��2Cu+O2
����ͭ��Ũ���ᷴӦ��Cu+4HNO3(Ũ)=Cu��NO3��2+2NO2��+2H2O����ͭ����������Ӧ��������ͭ������ͭ�ٸ����ᷴӦ��2Cu+O2![]() 2CuO��CuO+2HNO3= Cu��NO3��2+H2O��A��ͭԪ�ض�����������ͭ��������ȡ����������ͭ����ͭ��������ȣ�A��ȷ��B�����������ķ�Ӧ;����Ϸ�Ӧʽ��֪����;����������������ʵ�������>��>����B����C��;�������Ʊ�������ԭ����������ߣ���û����Ⱦ����������������������������ɫ��ѧ�����C��ȷ��D��;�����б�������ͭ�뱻��ԭ����������ʵ���֮����3��2��D��ȷ����ѡB��
2CuO��CuO+2HNO3= Cu��NO3��2+H2O��A��ͭԪ�ض�����������ͭ��������ȡ����������ͭ����ͭ��������ȣ�A��ȷ��B�����������ķ�Ӧ;����Ϸ�Ӧʽ��֪����;����������������ʵ�������>��>����B����C��;�������Ʊ�������ԭ����������ߣ���û����Ⱦ����������������������������ɫ��ѧ�����C��ȷ��D��;�����б�������ͭ�뱻��ԭ����������ʵ���֮����3��2��D��ȷ����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ķ�Ӧ·��������Ϣ��� 
��1��A�Ľṹ��ʽ�� �� B�Ľṹ��ʽ�� ��
��2����Ӧ�����õ��Լ��������� �� �÷�Ӧ������Ϊ ��
��3����Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ��ȷ���ǣ� ��
A.�����ȼ����Ϊ890.3KJ?mol��1 �� �����ȼ���ȵ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4��g��+2O2��g���TCO2��g��+2H2O��g����H=��890.3 kJ?mol��1
B.500�桢30 MPa �£���0.1 mol N2 �� 0.3 mol H2 �����ܱ������г�ַ�Ӧ����NH3��g��������3.86 KJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g�� ![]() ? 2NH3��g����H=��38.6 KJ?mol��1
? 2NH3��g����H=��38.6 KJ?mol��1
C.��֪1 gҺ̬�º�����Һ̬�������ⷴӦ���ɵ�����ˮ����ʱ�ų�20.05 kJ���������º������ⷴӦ���Ȼ�ѧ����ʽΪ��N2H4��l��+2H2O2��l���TN2��g��+4H2O��g����H=��641.6 KJ?mol��1
D.CO��g����ȼ������283.0 KJ?mol��1 �� ��2CO2��g���T2CO��g��+O2��g�� ��Ӧ�ġ�H=+283.0 KJ?mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ����д��ȷ����
A. Ư����Һ��ͨ��SO2���壺Ca2����2ClO����SO2��H2O===CaSO3����2HClO
B. ̼�������Һ�м������������������Һ��HCO![]() ��OH��===CO
��OH��===CO![]() ��H2O
��H2O
C. ��Fe2(SO4)3��Һ�м���������ۣ�2Fe3����Fe===3Fe2��
D. ��Na2SiO3��Һ�еμ�ϡ���Na2SiO3��2H��===H2SiO3����2Na��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ���������ȷ���ǣ� ��
A.����������ӵĻ�ѧʽ��ClO��
B.�ɱ��ķ���ʽ��H2O
C.��ϩ�Ľṹ��ʽ��CH2CH2
D.�Ҵ��Ľṹ��ʽ��C2H6O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڿ�ѧʷ�ϣ��й��������ش�ķ����ͷ��֣�Ϊ�����ִ����������춨�˻��������·����������ڻ�ѧʷ���й��������ش����ǣ� ��
����ֽ ��ӡˢ���� �ۻ�ҩ ��ָ���� ����ͭ������������ �ϳ��л��߷��Ӳ��� ���˹��ϳ�ţ�ȵ��� �����ԭ�ӡ���������ѧ˵
A.�٢ۢݢ�B.�ڢܢޢ�C.�ڢۢܢ�D.�ݢޢߢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A. �������������ﶼ����ֱ����ˮ��Ӧ���ɶ�Ӧ����
B. �ǽ��������ﶼ������������
C. ���������ﶼ�ǽ���������
D. ���������ﶼ�Ǽ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ����̼��ԭ����ͭ���Ʊ�����ͭ��Ҫ���¶Ƚϸߣ���ͨ�ƾ��ƺ��Ѵﵽ���¶ȣ�ijʵ��С������ˮ����ͭ��������ͭ��ֻ������ͨ�ƾ��Ƽ��ȷ�Ӧ���ܴﵽ��ͬ��ʵ��Ŀ�ģ������ɵĻ������ͨ������װ�ý��м��飬�Իش��������⣺ 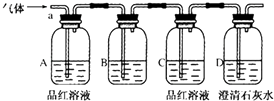
��1��A�е�Ʒ����Һ��ɫ��֤�������壻C��Ʒ����Һ����������D�еij���ʯ��ˮ����ǣ�֤�������壻
��2��B�пɼ��� �� �Գ�ȥ��������е�ij�����壻 a�����Ը��������Һ b������̼��������Һ
c�������Ȼ�����Һ d����ˮ
��3����������ʵ��������д��̼��ԭ����ͭ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com