
| A. | 全部由非金属元素组成的化合物中可含离子键 | |
| B. | H2O中所有原子都满足八电子稳定状态 | |
| C. | 两种元素构成的化合物可以含有非极性共价键 | |
| D. | CH4中所有的电子都参与形成共价键 |
分析 A.全部由非金属元素组成的化合物为共价化合物或离子化合物;
B、H2O中氢原子最外层达两电子的稳定结构;
C、氢与氧两种元素生成过氧化氢分子中含非极性共价键;
D、CH4中碳原子只有4个电子都参与形成共价键.
解答 解:A.全部由非金属元素组成的化合物为共价化合物或离子化合物,如HCl为共价化合物,氯化铵为离子化合物,故A正确;
B、H2O中氢原子最外层达两电子的稳定结构,而不是8电子,故B错误;
C、氢与氧两种元素生成过氧化氢分子中含非极性共价键氧氧键,故C正确;
D、CH4中碳原子只有4个电子都参与形成共价键,而不是所有原子,故D错误;
故选AC.
点评 本题考查化学键,离子化合物与共价化合物的区别,题目难度不大,注意相关基础知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | 足量Mg与2.8gN2完全反应后失去0.2NA电子 | |
| B. | 3.0g由葡萄糖和冰醋酸组成的混合物中含有的原子总数为0.3NA | |
| C. | 常温常压下,2.8gC2H4含有共用电子对的数目为0.6NA | |
| D. | 16gO2含有NA个18O原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 24:30 | B. | 60:24 | C. | 2:1 | D. | 1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该磁黄铁矿中FexS的x=0.425 | |
| B. | 生成的H2S气体在标准状况下的体积为2.24L | |
| C. | 100mL的盐酸中HCl物质的量浓度为8.5mol/L | |
| D. | 该磁黄铁矿FexS中,Fe2+与Fe3+的物质的量之比为3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S$\stackrel{O_{2}、点燃}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| B. | H2SO4(稀)$\stackrel{Cu}{→}$SO2$\stackrel{BaCl_{2}}{→}$BaSO4 | |
| C. | Fe2O3$\stackrel{盐酸}{→}$FeCl3(ap)$\stackrel{蒸发}{→}$无水FeCl3 | |
| D. | SiO2$\stackrel{NaOH}{→}$NaSiO3$\stackrel{HCl}{→}$H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
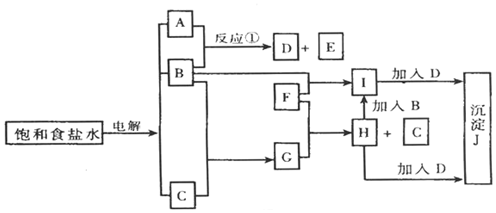
 ,G
,G ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4项 | B. | 3项 | C. | 2项 | D. | 1项 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2在反应中被还原成NaHSO4 | |
| B. | NaC1O3在反应中失去电子 | |
| C. | H2SO4在反应中作氧化剂 | |
| D. | 若反应中转移1mol电于,则生成1mol C1O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com