
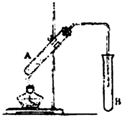
 在试管A中加入3mL乙醇,然后边振荡试管边慢慢加入2mL乙醇,如图连接好装置进行实验,以制取乙酸乙酯.
在试管A中加入3mL乙醇,然后边振荡试管边慢慢加入2mL乙醇,如图连接好装置进行实验,以制取乙酸乙酯.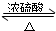 CH3COOC2H5+H2O,
CH3COOC2H5+H2O, CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O; CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:高中化学 来源: 题型:
 Ⅰ.乙酸是生活中常见的有机物之一,乙酸的官能团为
Ⅰ.乙酸是生活中常见的有机物之一,乙酸的官能团为 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O查看答案和解析>>
科目:高中化学 来源: 题型:
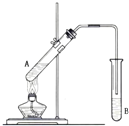 在试管A中加入3mL 乙醇,然后边振荡试管边慢慢加入2mL 浓硫酸和2mL 乙酸,按如图所示连接好装置进行实验,以制取乙酸乙酯.
在试管A中加入3mL 乙醇,然后边振荡试管边慢慢加入2mL 浓硫酸和2mL 乙酸,按如图所示连接好装置进行实验,以制取乙酸乙酯.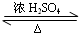 CH3COOC2H5+H2O
CH3COOC2H5+H2O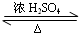 CH3COOC2H5+H2O
CH3COOC2H5+H2O查看答案和解析>>
科目:高中化学 来源: 题型:
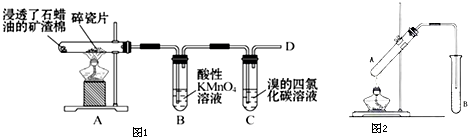
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com