

分析 (1)过滤除去不溶杂质,若温度冷却,硫化钠会结晶析出而损失;
(2)盛放Na2SO3固体的玻璃仪器是蒸馏烧瓶,三颈烧瓶内反应结束会有未反应的二氧化硫,直接排放会污染空气;
(3)①用配制的碘溶液滴定硫代硫酸钠,利用碘单质遇碘单质变蓝指示反应终点
②终点读数与起点读数之差为消耗碘的标准溶液体积,根据方程式计算
③局部变色就停止滴定,消耗标准溶液体积偏小,测定结果偏低.
解答 解:(1)过滤除去不溶杂质,若温度冷却,硫化钠会结晶析出而损失,
故答案为:防止硫化钠结晶析出而损失、去除杂质;
(2)盛放Na2SO3固体的玻璃仪器是蒸馏烧瓶,三颈烧瓶内反应结束会有未反应的二氧化硫,装置中氢氧化钠是吸收尾气的主要作用,因为原料气二氧化硫是污染性气体不能排放到空气中,以防止污染空气,
故答案为:蒸馏烧瓶;吸收SO2等尾气,防止污染;
(3)①用配制的碘溶液滴定硫代硫酸钠,滴入最后一滴碘的标准溶液,溶液变为蓝色,且30s内不恢复原色,说明反应到达终点,
故答案为:滴入最后一滴碘的标准溶液,溶液变为蓝色,且30s内不恢复原色;
②终点读数为18.10mL,起点读数为0.00mL,故消耗碘的标准溶液体积为18.10mL,
设Na2S2O3•5H2O的纯度为x,则:
2Na2S2O3•5H2O~2Na2S2O3~I2
2M g 1mol
Wxg 18.10×10-3L×0.1000 mol•L-1
故2M g:Wx g=1mol:18.10×10-3L×0.1000 mol•L-1
解得x=$\frac{0.362M}{W}$%,
故答案为:18.10;$\frac{0.362M}{W}$%;
③局部变色就停止滴定,消耗标准溶液体积偏小,会使样品中Na2S2O3•5H2O的纯度的测量结果偏低,
故答案为:偏低.
点评 本题考查实验方案方案,涉及探究温度和浓度对反应速率的影响、物质实验制备、氧化还原反应滴定等,是对学生综合能力的考查,难度中等.


科目:高中化学 来源: 题型:解答题
 某条件下,在2L密闭容器中充入NO2发生如下反应:2NO2(g)?
某条件下,在2L密闭容器中充入NO2发生如下反应:2NO2(g)?查看答案和解析>>
科目:高中化学 来源: 题型:选择题
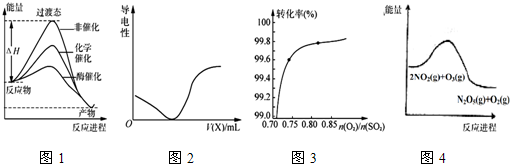
| A. | 由图1所示曲线可知,化学催化比酶催化的效果好 | |
| B. | 在H2S溶液导电性实验中,由图2所示曲线可确定通入的气体X为Cl2 | |
| C. | 其它条件不变,关于反应2SO2(g)+O2(g)$?_{加热}^{催化剂}$2SO3(g),图3中纵坐标表示O2的转化率 | |
| D. | 图4的反应升高温度,平衡常数减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9种 | B. | 12种 | C. | 15种 | D. | 18种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素都是活泼的金属元素 | |
| B. | 卤素是常见的成盐元素,都是氧化剂 | |
| C. | 卤素原子最外层都有7个电子 | |
| D. | 卤化氢、卤化银的性质都有相似之处 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温、常压下,11.2L N2含有的分子数为0.5NA | |
| B. | 标准状况下,18g H2O的体积是22.4L | |
| C. | NA个SO2的体积是22.4L | |
| D. | 标准状况下,22.4L H2 与O2的混合气体所含原子数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com