
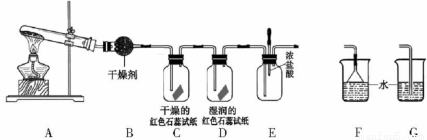
某中学化学研究性学习小组利用以下装置制取并探究氨气的性质。A中发生反应的化学方程式: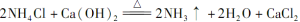
【实验探究】
(1)A中的反应 (填“是”或“不是”)氧化还原反应。
(2)A装置还可用于制取气体 (只填一种)
(3)若有10.7gNH4Cl固体,最多可制取NH3(标准状况)的体积是 L (NH4C1的摩尔质量为53.5g·mol-1)。
(4)实验室收集氨气的方法是
(5)C、D装置中颜色会发生变化的是 (填“C”或“D”)
(6)当实验进行一段时间后,挤压E装置中的胶头滴管,滴人1-2滴浓盐酸,可观察到的现象是
(7)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是 (填“F”或“G”)。
【知识拓展】
(8)生石灰与水反应生成Ca(OH)2并放出热量[化学方程式为CaO+H2O==Ca(OH)2]。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。你认为生石灰可用下列 物质代替(填序号)。
A.碱石灰(NaOH与CaO的固体混合物) B.NaOH 固体
C.硫酸溶液 D.石灰石(含CaCO3)
【知识应用】
(9)2010年11月9日晚,我省宁德市一冷冻厂发生氨气泄漏事件,500 多居民深夜大转移。假如你在现场,你会采用什么自救为法?
(1)不是 (2)02(或氧气,其他合理答案也给分)(3)4.48 (4)向下排空气法
(5)D (6)有白烟生成 (7)F (8)A B
(9)①用湿毛巾捂住口鼻,并迅速撤离。②低头弯腰,往低处跑,迅速撤离。③逆风奔跑,迅速撤离。④戴上防毒面具,迅速撤离。(以上任选其一或其他合理答案也给分)
【解析】
试题分析:(1)A装置是实验室制氨气,A中化学反应方程式2NH4Cl + Ca(OH)2  CaCl2 + 2NH3↑+ 2H2O,不是氧化还原反应。
CaCl2 + 2NH3↑+ 2H2O,不是氧化还原反应。
(2)A装置的特点是固体和固体加热制备气体的,所以还可以制备氧气。
(3)10.7 g NH4Cl固体的物质的量是10.7g÷53.5g/mol=0.2mol,则根据反应的化学方程式可知,生成氨气的体积是0.2mol×22.4L/mol=4.48L。
(4)氨气极易溶于水,且氨气的密度小于空气的,所以实验室收集氨气的方法是向下排空气法。
(5)氨气不能使干燥的红色石蕊试纸变蓝,所以C、D装置中颜色会发生变化的是D。
(6)浓盐酸和氨气反应生成氯化铵固体小颗粒,所以可观察到的现象是有白烟生成。
(7)氨气极易溶于水,进行尾气处理时,要防止倒吸,选F。
(8)碱石灰或氢氧化钠固体,均易吸水,且增大溶液中OH-离子的浓度,可用于代替生石灰,选AB。
考点:考查氨气的制备、收集、检验、尾气处理,化学计算等知识。


科目:高中化学 来源:2014-2015学年湖南省高二上学期期中化学(理)试卷(解析版) 题型:填空题
(12分,每空2分)(1)常温下,将0.2 mol/L HCl溶液与0.2 mol/L氨水等体积混合(忽略混合后溶液体积的变化),测得混合后溶液的pH=6,试回答以下问题:
(1)混合后溶液呈酸性的原因是(用离子方程式回答) 。
(2)混合后溶液中由水电离出的c(OH-)为
(3)常温下,将0.2 mol·L-1的盐酸与 0.2mol·L-1的氨水混合,若所得的混合溶液中的pH=7,下列关系正确的是
A、[Cl-]>[NH4+]> [H+] > [OH-]
B、[NH4+]>[Cl-]>[OH-]>[H+]
C、[Cl-]=[NH4+]>[H+]=[OH-]
D、[NH4+]>[Cl-]>[H+]>[OH-]
(4)由电离常数可知酸性强弱: CH3COOH>H2CO3>HCO3-,则浓度相同的下列溶液碱性由强到弱顺序为: (填序号)
①CH3COONa ②NaHCO3 ③Na2CO3
(5)将氯化铁溶液蒸干、灼烧,最后得到的固体是 。
(6)Cu(OH)2(s)  Cu2+(aq)+2OH-(aq),在常温下Ksp( Cu(OH)2)=2×10-20。在常温下如果要生成Cu(OH)2沉淀,需要向0.02 mol?L-1的CuSO4溶液中加入NaOH溶液,调整pH最小到 。
Cu2+(aq)+2OH-(aq),在常温下Ksp( Cu(OH)2)=2×10-20。在常温下如果要生成Cu(OH)2沉淀,需要向0.02 mol?L-1的CuSO4溶液中加入NaOH溶液,调整pH最小到 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省伊春市高一上学期期中化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.胶体区别于其他分散系的根本原因是胶体有丁达尔效应
B.氯化铁溶液加入到冷水中可以制得氢氧化铁胶体
C.分散系中分散质粒子直径由小到大的正确顺序是:溶液<胶体<浊液
D.胶体的分散质可以通过过滤从分散剂中分离出来
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省伊春市高二上学期期中化学试卷(解析版) 题型:选择题
可逆反应:2SO2+O2 2SO3,用一定量的SO2和O2在容积固定的密闭容器内发生反应,如果v(SO2)=0.05 mol/(L·min),则2 min后SO3的浓度为
2SO3,用一定量的SO2和O2在容积固定的密闭容器内发生反应,如果v(SO2)=0.05 mol/(L·min),则2 min后SO3的浓度为
A.1 mol/L B.0.9 mol/L C.0.2 mol/L D.0.1mol/L
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省伊春市高二上学期期中化学试卷(解析版) 题型:选择题
从如图所示的某气体反应的能量变化分析,以下判断错误的是

A.这是一个放热反应
B.该反应可能需要加热
C.生成物的总能量低于反应物的总能量
D.反应物比生成物更稳定
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高二上学期期中化学(文)试卷(解析版) 题型:选择题
3NO2十H2O==2HNO3十NO为工业上氨催化氧化法制硝酸的反应之一,该反应中NO2的作用是
A.只作氧化剂 B.作催化剂
C.既作氧化剂又作还原剂 D.作干燥剂
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高二上学期期中化学(理)试卷(解析版) 题型:选择题
在一容积可变的密闭容器中,aA(气) bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则
A.平衡向正反应方向移动了 B.物质A的转化率减少了
C.物质B的质量分数减小了 D.化学计量数关系a>b
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济宁市高三上学期期中化学试卷(解析版) 题型:填空题
(8分)某一离子反应体系有反应物和产物共以下六种:MnO4-、H+、O2、H2O、H2O2、Mn2+,
已知该反应中的H2O2只发生如下过程:
(1)该反应中的还原剂是 ,还原产物是________。
(2)KMnO4溶液随着酸性的增强氧化性不断增强,应选择_______(选填“稀硫酸”或“浓盐酸”)进行KMnO4溶液的酸化。
(3)假如反应转移了0.3mol电子,则产生的气体在标准状况下体积为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com