
| |||||||||||||||||||||||||||
(1) |
若用启普发生器制取气体,所选试剂应为块状固体和液体,且反应不需要加热,故 A、D选项正确,C选项错误.由于硝酸具有强氧化性,与硫化亚铁反应得不到硫化氢气体,B选项错误. |
(2) |
答案:②③④ 讲析:要控制硫化氢气体产生的速率,必须选用分液漏斗. |
(3) |
答案:品红溶液褪色;瓶壁上产生淡黄色的粉末和无色的小液滴 2H2S+SO2讲析:开始时氧气充足,硫化氢气体燃烧生成二氧化硫和水;之后氧气不足,燃烧产物为单质硫和水,描述反应现象时要从二氧化硫、单质硫、水三个方面加以考虑. |
(4) |
答案: B讲析: A选项增加的装置起不到任何作用.B选项的装置可将启普发生器内的硫化氢气体与点燃的硫化氢气体分开,能够防止爆炸.C、D选项的装置中生成的硫化氢气体无法排出,达不到实验目的.点评:本题将教材实验进行迁移,涉及了“固+液→气”的原理、还原性气体的性质以及点燃可燃性气体的注意事项等. |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
| 资料:①H2S可溶于水(约1:2),其水溶液为二元弱酸. ②H2S可与许多金属离子反应生成沉淀. ③H2S在空气中燃烧,火焰呈淡蓝色. |
| 实验操作 | 实验现象 | |
| 实验1 | 将等浓度的Na2S和Na2SO3溶液按体积比2:1混合 | 无明显现象 |
| 实验2 | 将H2S通入Na2SO3溶液中 | 未见明显沉淀,再加入少量稀硫酸,立即产生大量浅黄色沉淀 |
| 实验3 | 将SO2通入Na2S溶液中 | 有浅黄色沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 0.085cV |
| ρ |
| 0.085cV |
| ρ |
| 实 验 内 容 | 实 验 方 法 | 实 验 现 象 |
| 探究氧化性 | 取适量饱和硫化氢溶液于试管中,滴入 过氧化氢溶液.(取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液.) 取适量饱和硫化氢溶液于试管中,滴入 过氧化氢溶液.(取适量碘化钾淀粉溶液于试管中,加入过氧化氢溶液.) |
产生淡黄色沉淀或溶液变浑浊.(溶液变蓝色.) 产生淡黄色沉淀或溶液变浑浊.(溶液变蓝色.) |
| 或探究不稳定性 | 取适量过氧化氢溶液于试管中,加热, 用带火星的木条检验.(取适量过氧化氢溶液于试管中,加热,用导气管将得到的气体通入到装有饱和硫化氢溶液的试管中.) 取适量过氧化氢溶液于试管中,加热, 用带火星的木条检验.(取适量过氧化氢溶液于试管中,加热,用导气管将得到的气体通入到装有饱和硫化氢溶液的试管中.) |
产生气泡,木条复燃.(溶液变浑浊或有浅黄色沉淀产生) 产生气泡,木条复燃.(溶液变浑浊或有浅黄色沉淀产生) |
查看答案和解析>>
科目:高中化学 来源:志鸿系列必修一训练化学苏教版 苏教版 题型:058
已知:①FeS不溶解于水 ②实验室制取H2S、SO2气体的原理是FeS+H2SO4![]() FeSO4+H2S↑,Na2SO3+H2SO4
FeSO4+H2S↑,Na2SO3+H2SO4![]() Na2SO4+H2O+SO2↑ ③硫化氢与二氧化硫气体相遇会发生反应:2H2S+SO2
Na2SO4+H2O+SO2↑ ③硫化氢与二氧化硫气体相遇会发生反应:2H2S+SO2![]() 3S↓+2H2O.
3S↓+2H2O.
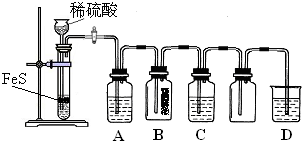
根据下图中的实验装置和试剂进行实验,完成下列问题:

(1)装置A是由双孔塞、玻璃导管及________和________组装起来的.
(2)组装一套制取SO2气体的装置,并证明SO2既有氧化性,又有还原性和漂白性.
①按实验装置连接顺序,把a→f各导管口连接起来,正确的顺序有________.
A.befcda
B.adcefb
C.acdfeb
D.acdefb
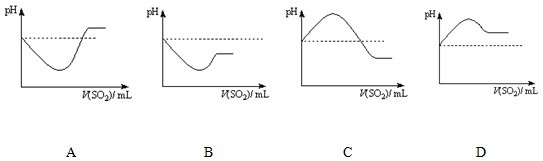
②若C装置中的溶液为________,反应后该溶液变为无色,说明SO2具有还原性.
③若C装置中的溶液为________,反应后该溶液变为无色,说明SO2具有漂白性.
④当D中产生________现象时,说明SO2具有氧化性.
(3)D装置烧杯中NaOH溶液的作用是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
(08年上海卷)![]() 设计学生实验要注意安全、无污染、现象明显。根据启普发生器原理,可用底部有小孔的试管制简易的气体发生器(见右图)。若关闭K,不能使反应停止,可将试管从烧杯中取出(会有部分气体逸散)。下列气体的制取宜使用该装置的是( )
设计学生实验要注意安全、无污染、现象明显。根据启普发生器原理,可用底部有小孔的试管制简易的气体发生器(见右图)。若关闭K,不能使反应停止,可将试管从烧杯中取出(会有部分气体逸散)。下列气体的制取宜使用该装置的是( )
A.用二氧化锰(粉末)与双氧水制氧气 B.用锌粒与稀硫酸制氢气
C.用硫化亚铁(块状)与盐酸制硫化氢 D.用碳酸钙(块状)与稀硫酸制二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)实验室制取硫化氢的化学方程式____________________________________。
(2)根据装置图完成下列问题。

①制取硫化氢气体的发生装置可以选用_____________。
②若用C装置收集硫化氢气体,进气口应为_____________,原因是___________________。
③为了验证硫化氢的水溶液呈酸性,可以将气体通入装置D,D中所盛的试剂应该是_____________,现象是_______________________。
④做上述实验时,为了防止多余的硫化氢逸出污染环境,可以将其通入装置E吸收,E中漏斗的作用为____________________________。
⑤整套装置的连接口连接顺序为(填写a、b、c等符号)____________________。
(3)现用
①收集到的H2S气体的体积(标准状况)。
②溶液中Fe2+和H+的物质的量浓度。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com