
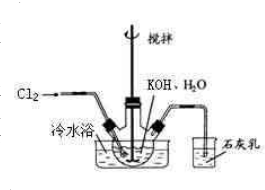
 ��ˮԡ��ȴ��ͨ��Cl2���õ綯���������Ͻ��裬ֱ����Һ��Ϊ����ɫ����������ɫ��������Ϊֹ���ڽ����ʹ�����ص����ձ���������ˮԡ�У��ڲ��Ͻ����£��ּ��μ���130gKOH���壮�ò���ɰо©�����ˣ���ȥ��������Ҫ�ɷ�ΪKCl������KOH��KClO�����ô������ǿ���Ա�����Һ��
��ˮԡ��ȴ��ͨ��Cl2���õ綯���������Ͻ��裬ֱ����Һ��Ϊ����ɫ����������ɫ��������Ϊֹ���ڽ����ʹ�����ص����ձ���������ˮԡ�У��ڲ��Ͻ����£��ּ��μ���130gKOH���壮�ò���ɰо©�����ˣ���ȥ��������Ҫ�ɷ�ΪKCl������KOH��KClO�����ô������ǿ���Ա�����Һ�� 5KCl+KClO3+3H2O�������˴�����صIJ�����
5KCl+KClO3+3H2O�������˴�����صIJ����� 5KCl+KClO3+3H2O�������˴�����صIJ�����
5KCl+KClO3+3H2O�������˴�����صIJ�����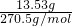 =0.05mol��������Ԫ���غ��֪n��K2FeO4��=0.05mol������m��K2FeO4��=0.05mol��198g/mol=9.9g��
=0.05mol��������Ԫ���غ��֪n��K2FeO4��=0.05mol������m��K2FeO4��=0.05mol��198g/mol=9.9g��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
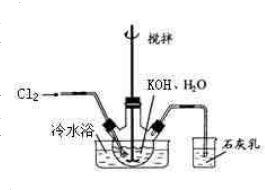 ��ˮԡ��ȴ��ͨ��Cl2���õ綯���������Ͻ��裬ֱ����Һ��Ϊ����ɫ����������ɫ��������Ϊֹ���ڽ����ʹ�����ص����ձ���������ˮԡ�У��ڲ��Ͻ����£��ּ��μ���130gKOH���壮�ò���ɰо©�����ˣ���ȥ��������Ҫ�ɷ�ΪKCl������KOH��KClO�����ô������ǿ���Ա�����Һ��
��ˮԡ��ȴ��ͨ��Cl2���õ綯���������Ͻ��裬ֱ����Һ��Ϊ����ɫ����������ɫ��������Ϊֹ���ڽ����ʹ�����ص����ձ���������ˮԡ�У��ڲ��Ͻ����£��ּ��μ���130gKOH���壮�ò���ɰо©�����ˣ���ȥ��������Ҫ�ɷ�ΪKCl������KOH��KClO�����ô������ǿ���Ա�����Һ�� 5KCl+KClO3+3H2O��
5KCl+KClO3+3H2O�� 5KCl+KClO3+3H2O��
5KCl+KClO3+3H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011�꽭��ʡ�����и�����ѧ�߿���ѧģ���Ծ��������������棩 ���ͣ������
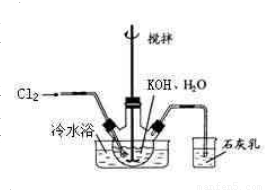 ��ˮԡ��ȴ��ͨ��Cl2���õ綯���������Ͻ��裬ֱ����Һ��Ϊ����ɫ����������ɫ��������Ϊֹ���ڽ����ʹ�����ص����ձ���������ˮԡ�У��ڲ��Ͻ����£��ּ��μ���130gKOH���壮�ò���ɰо©�����ˣ���ȥ��������Ҫ�ɷ�ΪKCl������KOH��KClO�����ô������ǿ���Ա�����Һ��
��ˮԡ��ȴ��ͨ��Cl2���õ綯���������Ͻ��裬ֱ����Һ��Ϊ����ɫ����������ɫ��������Ϊֹ���ڽ����ʹ�����ص����ձ���������ˮԡ�У��ڲ��Ͻ����£��ּ��μ���130gKOH���壮�ò���ɰо©�����ˣ���ȥ��������Ҫ�ɷ�ΪKCl������KOH��KClO�����ô������ǿ���Ա�����Һ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com