
【题目】下列化合物,既有离子键也有共价键的是( )
A.氯化氢 B.硫酸 C.氯化铵 D.乙酸
科目:高中化学 来源: 题型:
【题目】化学与人类生活、社会可持续发展密切相关。下列措施有利于节能减排、保护环境的是( )
①加快化石燃料的开采与使用;
②研发易降解的生物农药;
③应用高效洁净的能源转换技术;
④田间焚烧秸秆;
⑤推广使用节能环保材料.
A. ①③⑤ B. ②③⑤ C. ①②④ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:硫酸铜溶液中滴入氨基乙酸钠(H2N-CH2-COONa)即可得到配合物A。其结构如图4所示:
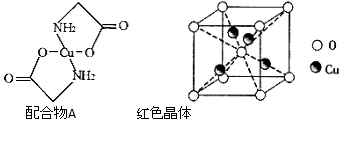
(1)Cu元素基态原子的外围电子排布式为 。
(2)元素C、N、O的第一电离能由大到小排列顺序为 。
(3)配合物A中碳原子的轨道杂化类型为 。
(4)1mol氨基乙酸钠(H2N-CH2-COONa)含有![]() 键的数目为 mol。
键的数目为 mol。
(5)氨基乙酸钠分解产物之一为二氧化碳。写出二氧化碳的一种等电子体: (写化学式)。
(6)已知:硫酸铜灼烧可以生成一种红色晶体,其结构如图5所示,则该化合物的化学式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用含少量镁粉的铝粉制取纯净的氢氧化铝,下述操作步骤中最恰当的组合是
①加盐酸溶解 ②加烧碱溶液溶解 ③过滤 ④通入过量CO2生成Al(OH)3沉淀
⑤加入盐酸,生成Al(OH)3沉淀⑥加入过量烧碱溶液
A.①⑥⑤③ B.②③④③
C.②③⑤③ D.①③⑤③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A是石油裂解气的主要成份,能使溴水褪色;A是一种重要的化工原料,它的产量通常用来衡量一个国家石油化工水平.现以A为主要原料合成乙酸乙酯及高分子化合物E,其合成路线如图所示:

请回答下列问题:
(1)写出A的电子式 .
(2)B、D分子中的官能团名称分别是 、 .
(3)写出下列反应的化学方程式并指出反应类型:
① 反应类型 ;
② 反应类型 ;
④ 反应类型 。
⑤ 反应类型 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒,国际上对食品中亚硝酸钠的用量控制在很低的水平上。某学习小组针对亚硝酸钠设计了如下实验:
【实验I】制备NaNO2
该小组查阅资料知:2N0+Na2O2=2NaNO2;2NO2+Na2O2=2NaNO3。
设计制备装置如下(夹持装置略去)。
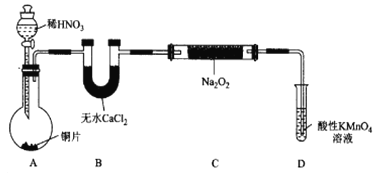
(1)装置D可将剩余的NO氧化成NO3-,发生反应的离子方程式为_______________。
(2)如果没有B装置,C中发生的副反应有____________。
(3)甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质。于是在A 与B 装且间增加了___________装置,改进后提高了NaNO2的纯度。
【实脸II】 测定制取的样品中NaNO2的含量
步骤:
A.在5个有编号的带刻度试管(比色管)中分别加人不同址的NaNO2溶液,各加入1 ml的M溶液(M遇NaNO2呈紫红色,NaNO2浓度越大颜色越深),再加蒸馏水至总体积均为10 mL并振荡,制成标准色阶:
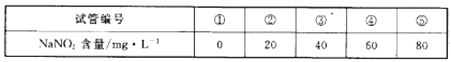
b.称量0.10g制得的样品溶于水配成500 ml溶液。取5mL待测液,加入1mlM溶液,后加蒸馏水至10mL振荡,与标准色阶比较。
(4)步脚b中比较结果:待测液颜色与③号色阶相同。则甲同学制得的样品中NaNO2的质量分数是______%。
(5)用目视比色法证明维生素C可以有效降低NaNO2的含量。设计并完成下列实验报告。
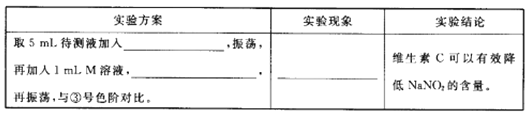
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A.在0.1 mol NaHSO4晶体中阳离子与阴离子总数为0.3NA
B.25℃时,pH=13的1.0 LBa(0H)2溶液中含有的OH-数目为0.2NA
C.常温常压下,4.4gCO2和N2O混合物中所含有的原子数为0.3 NA
D.1L1 mol·L-1FeCl3完全水解生成NA个胶体粒子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积为VL的密闭容器中进行反应:aN(g)![]() bM(g),M、N的物质的量随时间的变化曲线如图所示。
bM(g),M、N的物质的量随时间的变化曲线如图所示。
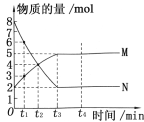
(1)该反应的化学方程式中= 。
(2)t1~t2时间段,以M的浓度变化表示的平均反应速率为 。
(3)t2时,生成M的速率与消耗N的速率 (填“相等”或“不相等”)。
(4)下列叙述中能说明上述反应达到平衡状态的是 。
A.反应中M与N的物质的量之比为1∶1
B.混合气体的总物质的量不随时间的变化而变化
C.单位时间内每消耗a mol N,同时生成b mol M
D.N的质量分数在混合气体中保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]
对羟基苯甲酸丁酯(俗称尼泊金丁酯)可用作防腐剂,对酵母和霉菌有很强的抑制作用,工业上常用对羟基苯甲酸与丁醇在浓硫酸催化下进行酯化反应而制得。出下是某课题组开发的从廉价、易得的化工原料出发制备对羟基苯甲酸丁酯的合成路线:
①通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基;
②D可与银氨溶液反应生成银镜;
③F的核磁共振氢谱表明其有两种不同化学环境的氢,且峰面积比为l :1。
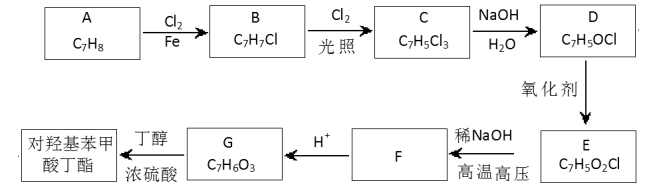
答下列问题:
(1)A的化学名称为 ;
(2)由B生成C的化学反应方程式为 ;
该反应的类型为 ;
(3)D的结构简式为 ;
(4)F的分子式为 ;
(5)G的结构简式为 ;
(6)E的同分异构体中含有苯环且能发生银镜反应的共有 种,其中核磁共振氢谱有三种不同化学环境的氢,且峰面积比为2:2:1,的是 (写结构简式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com