
【题目】下列属于酸的是( )
A.CO2B.CH3COOHC.K2CO3D.NaOH
科目:高中化学 来源: 题型:
【题目】已知:
H2(g)+ ![]() O2(g)═H2O(l)△H=﹣285.8kJ/mol;
O2(g)═H2O(l)△H=﹣285.8kJ/mol;
C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=﹣2220.0kJ/mol;
H2O(l)═H2O(g)△H=+44.0kJ/mol.
(1)写出丙烷燃烧生成CO2和气态水的热化学方程式:
(2)实验测得H2和C3H8的混合气体共5mol,完全燃烧生成液态水时放热6262.5kj,则混合气体中H2和C3H8的体积比为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁有δ、γ、α三种晶体结构,以下依次是δ、γ、α三种晶体在不同温度下转化的图示。下列有关说法中不正确的是 ( )
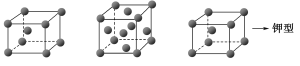
δ-Fe![]() γ-Fe
γ-Fe![]() α-Fe
α-Fe
A.δ-Fe晶体与每个Fe原子距离相等且最近的Fe原子有8个
B.γ-Fe晶体与每个Fe原子距离相等且最近的Fe原子有12个
C.图中α-Fe晶胞边长若为a cm,δ-Fe晶胞边长若为b cm,则两种晶体的密度比为b3:a3
D.将Fe加热到1 500℃分别急速冷却和缓慢冷却,得到的晶体类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为元素周期表中短周期主族非金属元素的一部分,下列说法不正确的是( )
X | Y |
Z | W |
A.W的原子序数可能是Y的两倍
B.Z的原子半径比Y的大
C.Y元素的非金属性比X元素的强
D.Z、W的氧化物对应的水化物均为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保证食品安全、保持营养均衡,是保障人体健康的基础.
①人体所需的元素从食物中摄取不足时,可通过食品添加剂和保健药剂以补充.如制成补钙、补锌的保健药剂或制成加碘食盐等,来增加对这些元素的摄入量.从上面提到的补钙剂、补锌剂和加碘食盐中的钙、锌、碘是指(填选项字母).
A.单质 B.原子 C.元素 D.离子
②被霉菌污染的粮食会产生黄曲霉素(C17H12O6),人类的特殊基因在黄曲霉素作用下会发生突变,继而诱发癌症.黄曲霉素属于(填“无机物”或“有机物”),
③由于化学物质使用不当,给人印象不佳的化学名词越来越多:苏丹红、三聚氰胺、….下列做法不会危及人体健康的是(填字母).
A.用甲醛浸泡海鲜产品 B.用霉变花生压榨食用油
C.用小苏打做糕点的疏松剂 D.用工业盐亚硝酸钠腌渍鱼肉
④碳酸氢钠是常用的疏松剂,它们在加热条件下产生气体,使食品变得疏松.请写出相关反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【实验化学】 偶氮苯是橙红色晶体,溶于乙醇,微溶于水,广泛应用于染料制造和橡胶工业,以硝基苯、镁粉和甲醇为原料制造偶氮苯的实验步骤如下:
步骤一:在反应器中加入一定量的硝基苯、甲醇和一小粒碘,装上冷凝管:加入少量镁粉,立即发生反应.
步骤二:等大部分镁粉反应完全后,再加入镁粉,反应继续进行,等镁粉完全反应后,加热回流30min.
步骤三:将所得液体趁热倒入冰水中,并不断搅拌,用冰醋酸小心中和至pH为4~5,析出橙红色固体,过滤,用少量冰水洗涤.
步骤四:用95%的乙醇重结晶.
(1)步骤一中反应不需要加热就能剧烈进行,原因是 . 镁粉分两次加入而不是一次性全部加入的原因是 .
(2)步骤三中析出固体用冰水洗涤的原因是 . 若要回收甲醇,实验所需的玻璃仪器除冷凝管、酒精灯、牛角管(应接管)和锥形瓶外还应有 .
(3)取0.1g偶氮苯,溶于5mL左右的苯中,将溶液分成两等份,分别装于两个试管中,其中一个试管用黑纸包好放在阴暗处,另一个则放在阳光下照射.用毛细管各取上述两试管中的溶液点在距离滤纸条末端1cm处,再将滤纸条末端浸入装有1:3的苯环己烷溶液的容器中,实验操作及现象如图所示. ①实验中分离物质所采用的方法是法.
②由实验结果可知:;利用该方法可以提纯反式偶氮苯.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案设计中,可行的是
A. 加过量稀盐酸后过滤,可除去混在铜粉中的少量镁粉和铝粉
B. 用萃取的方法可将汽油和煤抽进行分离
C. 用溶解、过滤的方法可分离硝酸钾和氯化钠固体混合物
D. 将混有氢气的氧气通过灼热的氧化铜,以除去其中的氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图所示。


可能用到的相关数据如下:
相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.961 8 | 161 | 微溶于水 |
环己烯 | 82 | 0.810 2 | 83 | 难溶于水 |
合成反应:
在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸。b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10 g。
回答下列问题:
(1)装置b的名称是____________。
(2)加入碎瓷片的作用是______________;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是________(填正确答案标号)。
A.立即补加 B.冷却后补加
C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并________;在本实验分离过程中,产物应该从分液漏斗的________(填“上口倒出”或“下口放出”)。
(4)分离提纯过程中加入无水氯化钙的目的是______________。
(5)在环己烯粗产物蒸馏过程中,不可能用到的仪器有________(填正确答案标号)。
A.圆底烧瓶
B.温度计
C.吸滤瓶
D.球形冷凝管
E.接收器
(6)本实验所得到的环己烯产率是________(填正确答案标号)。
A.41% B.50%
C.61% D.70%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com