
����Ŀ��һ������ȼ�ϵ�أ������������������缫����KOH��Һ�У�Ȼ���������Ϸֱ�ͨ��������������ط�ӦΪ��X����CH4+10OH��![]() 8e����CO32��+7H2O ��Y����4H2O+2O2+8e����8OH�������й��ڴ�ȼ�ϵ�ص��й�˵���д�����ǣ� ��
8e����CO32��+7H2O ��Y����4H2O+2O2+8e����8OH�������й��ڴ�ȼ�ϵ�ص��й�˵���д�����ǣ� ��
A. ͨ������ĵ缫��X��Ϊ��صĸ�����ͨ�������ĵ缫��Y��Ϊ�������
B. �ŵ�һ��ʱ��������Һ��KOH�����ʵ����ı�
C. �ڱ�״���£�ͨ��5.6L��������ȫ��Ӧ����1.0mol�ĵ��ӷ���ת��
D. �ŵ�ʱ��ͨ�������һ��������pH����
���𰸡�D
��������
�������ȼ�ϵ�ع���ʱ������������ԭ��Ӧ���缫��ӦʽΪO2+4e-+2H2O=4OH-�������ڸ�������������Ӧ���缫��ӦʽΪCH4+10OH--8e-=CO32-+7H2O����ϵ缫����ʽ�Լ���ĿҪ��ɽ����⡣
A. ����ԭ����ܷ�Ӧʽ��֪���鱻������Ϊԭ��صĸ�����Ӧ�������õ��ӱ���ԭ��ӦΪԭ��ص�������Ӧ����ͨ������ĵ缫(X)Ϊ��صĸ�����ͨ�������ĵ缫(Y)Ϊ���������A����ȷ��
B. ��������������ת������ȵõ���Ӧ���ܷ���ʽΪCH4+2O2+2OH�TCO32+2H2O��֪��Ӧ����KOH����������Һ��KOH�����ʵ����ı䣬B����ȷ��
C. n(O2)=![]() = 0.25 mol��ת�Ƶ��ӵ����ʵ���Ϊ0.25mol�� 4=1.0 mol��C����ȷ��
= 0.25 mol��ת�Ƶ��ӵ����ʵ���Ϊ0.25mol�� 4=1.0 mol��C����ȷ��
D. �����ڸ�������������Ӧ���������⣬ͨ������缫�ĵ缫��ӦΪCH4+10OH��![]() 8e����CO32��+7H2O�������������������ӣ����Էŵ�ʱ��ͨ�������һ��������pH���ͣ�D�����
8e����CO32��+7H2O�������������������ӣ����Էŵ�ʱ��ͨ�������һ��������pH���ͣ�D�����
��ѡD��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100mL MgCl2��AlCl3�Ļ����Һ�У���μ���NaOH��Һֱ�����������ⶨ������NaOH���ʵ��������ó��������ʵ����Ĺ�ϵ��ͼ��ʾ���ش��������⡣
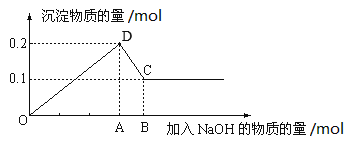
(1)ͼ��CD�η�Ӧ�Ļ�ѧ����ʽΪ___________��C����ڵĹ�������Ϊ________��
(2)A�������Ϊ_______�����Һ�У�MgCl2��Ũ��Ϊ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й��Ĵ����������磬�Ʊ��մ��������[��Ҫ�ɷ�Al2Si2O5(OH)4]Ϊԭ�ϣ��������ս���ɡ�������������ʽ��ʾ�������ɣ�ӦдΪ��________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ���ձ���ʢ��Ũ���ᣬ���ձ��ڷ�����ͭ�����ӵ�����Ǧ�����缫����֪��ԭ���ֹͣ����ʱ��Fe��Pb����ʣ�ࡣ����˵����ȷ���ǣ� ��
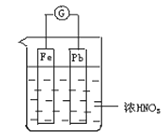
A. Fe��Pb���ã�ʼ��������
B. Fe��Ũ�����жۻ�ʼ�ղ��ܽ⡣
C. ���ֹͣ����ʱ����Fe(NO3)3����
D. ����Ũ���������Һ�����ϡ���ɫ��ѧ����˼��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij̼���ƺ�̼�����ƻ������ȡm g������Ʒ���м�������ȫ�ֽ����CO2112 mL����ȡm g������Ʒ����ˮ����������Һ����μ���150 mLϡ����ʱ����CO2 112 mL������ʱ����CO2 448 mL(���������Ϊ��״���²ⶨ)��
(1)̼��������̼���Ƶ����ʵ���֮��Ϊ____________________________________________��
(2)�������ʵ���Ũ��Ϊ______________(����2λ��Ч����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������20 mL 0.1 mol/L HA��Һ����μ���0.1 mol/L NaOH��Һ����pH�仯������ͼ��ʾ(�����¶ȱ仯)������˵���в���ȷ����

A. �����֪HAΪ����
B. �ζ��յ�λ��c��d֮��
C. �ζ���b��ʱ��n(Na+)+ n(H+)��n(OH��)+ n(HA)=0.002 mol
D. �ζ���d��ʱ��c(OH��)��c(Na+)��c(A��) ��c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������֤������������һ���������Ӽ�����(����)
A.������ˮB.���нϸߵ��۵�
C.����״̬���ܵ���D.����ˮ�ܵ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л��� a(![]() )��b(
)��b(![]() )��c(
)��c(![]() )��˵����ȷ����
)��˵����ȷ����
A. a��b��c �ķ���ʽ��Ϊ C8H8
B. a��b��c ��������ˮ������Ӧ
C. a��b��c ��ֻ�� a ������ԭ�ӿ��ܻᴦ��ͬһƽ��
D. a��b��c ��һ�ȴ����У�b �� 1 �֣�a��c ���� 5 ��(�����������칹)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������������ȷ���� (����)
A. 1 mol NH![]() ���еĵ�����Ϊ10NA
���еĵ�����Ϊ10NA
B. ��״���£�0.1 mol Cl2����ˮ��ת�Ƶĵ�����ĿΪ0.1NA
C. 1 L 0.1 mol��L��1��ˮ����0.1NA��OH��
D. 50 mL 18.4 mol��L��1Ũ����������ͭ�ȷ�Ӧ������SO2���ӵ���ĿΪ0.46NA
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com