
在25℃时,有pH为a的HCl溶液和pH为b的NaOH溶液,取VaL该盐酸溶液用该NaOH溶液中和,需VbL NaOH溶液,(题中a≤b,b≥8)。问:
(1)若a+b=14,则Va/Vb= .
(2)若a+b=13,则Va/Vb=
(3)若a+b>14,则Va/Vb= ,且Va Vb(填“>”“<”“=”)
科目:高中化学 来源: 题型:
下列反应达到化学平衡后,加压或降温都能使化学平衡向逆反应方向移动的是( )
A.2NO2(g) N2O4(g) ΔH<0 B.C(s)+CO2(g)
N2O4(g) ΔH<0 B.C(s)+CO2(g) 2CO(g) ΔH>0
2CO(g) ΔH>0
C.N2(g)+3H2(g) 2NH3(g) ΔH<0 D.H2S(g)
2NH3(g) ΔH<0 D.H2S(g) H2(g)+S(s) ΔH>0
H2(g)+S(s) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)向某溶液中加入KSCN溶液无明显现象,再滴入数滴氯水后,溶液立即变成红色,则原溶液中一定含有________离子,要除去FeCl3溶液中少量的氯化亚铁,可行的办法是________(填字母)。
A.加入铜粉 B.加入铁粉 C.通入氯气 D.加入KSCN溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式
________________________ _______。
(2)电子工业常用30%的FeCl3溶液腐蚀铜箔,制造印刷线路板,写出FeCl3与金属铜反应的离子方程式____________ __________________________。
(3)使用过的腐蚀液会失效,但可以回收利用,某兴趣小组为了从使用过的腐蚀液中回收铜,应使用的试剂是________(填字母)。
A.铜粉 B.氯气 C.铁粉 D.KSCN溶液
(4)向沸水中逐滴滴加1 mol·L-1FeCl3溶液至液体呈透明的红褐色,该分散系中微粒直径的范围是
___ ______nm,区别该液体和FeCl3溶液可用 方法。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在一容积可变的容器中,反应2A(g)+B(g) 2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、2 mol和4 mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
2C(g)达到平衡时,A、B和C的物质的量分别为4 mol、2 mol和4 mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
A.均减半 B.均加倍 C.均增加1 mol D.均减少1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
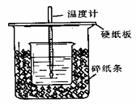 (1)从实验装置上看,图中尚缺少的一种
(1)从实验装置上看,图中尚缺少的一种
玻璃仪器是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (偏大、偏小、无影响)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;(填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
反应4NH3+5O2  4NO+6H2O在一定体积的密闭容器中进行,30 s后NO的物质的量浓度增加了3 mol/L,则下列反应速率正确的是
4NO+6H2O在一定体积的密闭容器中进行,30 s后NO的物质的量浓度增加了3 mol/L,则下列反应速率正确的是
A.v (NO)=0.02 mol·(L·s)-1 B.v (NO)=0.2mol·(L·s)-1
C.v (NH3)=0.01 mol·(L·s)-1 D.v (NH3)=0.1 mol·(L·s)-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.c(H+)等于1×10-7 mol/L的溶液一定是中性溶液
B.任何浓度的溶液都可以用pH来表示其酸性的强弱
C.无论是纯水、酸性、碱性或中性稀溶液,常温下,其c(H+)·c(OH-)=1×10-14
D.0.2 mol/L CH3COOH溶液中的c(H+)是0.1 mol/L CH3COOH溶液中的c(H+)的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
在温度不变下,在恒压容器a与恒容容器b中,分别充入体积比为1:3的N2和H2.若开始时两容器的体积相等,且在相同条件下达到平衡时,两容器中N2的转化率应当是( )
|
| A. | a中大 | B. | b中大 | C. | a、b一样大 | D. | 无法判断 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com