
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol/L H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
分析 (1)锌较活泼,可与硫酸铜、硫酸等发生置换反应;
(2)硫酸铜溶液加快氢气生成的速率,原因是形成原电池;
(3)在几种溶液中,只有银能被锌置换出来;
(4)影响化学反应速率的外界因素有温度、浓度、接触面积等;
(5)①为保证实验有对比性,只能逐渐改变一个变量分析,CuSO4溶液体积逐渐增多,故H2SO4的量应相等均为30mL,水的量减小,但每组实验中CuSO4与水的体积之和应相等;
②锌与硫酸反应使锌的表面凹凸不平,有很多细小的锌的颗粒,由于颗粒很小,光被完全吸收,所以看到的固体是灰黑色;Zn能够置换出Cu,出现紫红色;
③生成的单质Cu会沉积在Zn的表面,影响了反应速率.
解答 解:(1)因为Cu2+的氧化性比H+的强,所以加入硫酸铜,Zn先跟硫酸铜反应,反应完后再与酸反应,有关方程式为Zn+CuSO4=ZnSO4+Cu、Zn+H2SO4=ZnSO4+H2↑,
故答案为:Zn+CuSO4=ZnSO4+Cu、Zn+H2SO4=ZnSO4+H2↑;
(2)锌为活泼金属,加入硫酸铜,发生Zn+CuSO4=ZnSO4+Cu,置换出铜,与锌形成原电池反应,化学反应速率加快,
故答案为:CuSO4与Zn反应产生的Cu与Zn形成Cu-Zn-稀硫酸原电池,加快了氢气产生的速率;
(3)在几种溶液中,只有银能被锌置换出来,所以与CuSO4溶液起相似作用的是Ag2SO4溶液,
故答案为:Ag2SO4;
(4)要加快上述实验中气体产生的速率,还可采取的措施有:升高反应温度、适当增加硫酸的浓度、增加锌粒的表面积等,
故答案为:升高反应温度、适当增加硫酸的浓度、增加锌粒的表面积;
(5)①要对比试验效果,那么除了反应的物质的量不一样以外,要保证其它条件相同,而且是探究硫酸铜量的影响,那么每组硫酸的量要保持相同,六组反应的总体积也应该相同.A组中硫酸为30ml,那么其它组硫酸量也都为30ml.而硫酸铜溶液和水的总量应相同,F组中硫酸铜20ml,水为0,那么总量为20ml,所以V6=10ml,V9=17.5ml,V1=30ml,
故答案为:30;10;17.5;
②A中没有加入硫酸铜,锌与稀硫酸反应后,锌的表面凹凸不平,有很多细小的锌的颗粒,由于颗粒很小,光被完全吸收,所以看到的固体是灰黑色;Zn能够置换出Cu附着在Zn表面,金属变为紫红色,
故答案为:灰黑色;紫红色;
③因为锌会先与硫酸铜反应,直至硫酸铜反应完才与硫酸反应生成氢气,硫酸铜量较多时,反应时间较长,而且生成的铜会附着在锌片上,会阻碍锌片与硫酸继续反应,氢气生成速率下降,
故答案为:当加入一定量的硫酸铜后,生成的单质铜会沉积在锌的表面,降低了锌与溶液的接触面积.
点评 本题考查了影响化学反应速率的因素,并且融合了化学实验,形式新颖灵活,本题的易错点在于第(5)小题,首先V1、V6、V9的求得要注意分析表中数据;最后一问应该能够想到“覆盖”的问题,题目难度中等.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 电池反应的化学方程式为:CH3CH2OH+O2═CH3COOH+H2O | |
| B. | 检测时,电解质溶液中的 H+向负极移动 | |
| C. | 若有 0.4 mol 电子转移,则在标准状况下消耗 4.48 L 氧气 | |
| D. | 正极上发生的反应为:O2+4e-+2H2O═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
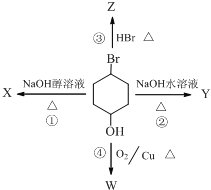 如图表示4-溴-1-环己醇所发生的4个不同反应,若生成物只含有一种官能团,则全部符合条件的反应有( )
如图表示4-溴-1-环己醇所发生的4个不同反应,若生成物只含有一种官能团,则全部符合条件的反应有( )| A. | ①④ | B. | ②③ | C. | ①②③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
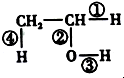 (1)在烷烃分子中,每增加一个碳原子,1mol 烷烃完全燃烧需要多消耗氧气(填字母)B.
(1)在烷烃分子中,每增加一个碳原子,1mol 烷烃完全燃烧需要多消耗氧气(填字母)B.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C3H6与C5H10 | B. | C3H8与C5H12 | C. | C2H6O与C5H8O | D. | C7H8与C6H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原性:Na>Mg>Al>Fe | B. | 碱性:NaOH>KOH>Ca(OH)2 | ||
| C. | 稳定性:HF>HCl>HBr>HI | D. | 酸性:HClO4>H2SO4>CH3COOH>H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl | |
| B. | CH2═CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl | |
| C. | CH3COOC2H5+H2O$?_{△}^{H+}$CH3COOH+C2H5OH | |
| D. | CH2═CH2+H2$→_{△}^{Ni}$CH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com