
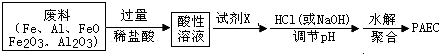
���� �����м������ϡ���ᣬ��ַ�Ӧ��õ�����Һ������Һ�к���AlCl3������Al��Fe�Լ�Fe2O3�����ʵ�����ϵ��ȷ��������ȷ����Һ��FeԪ�صĴ����γɣ�����ȷ���Ƿ����Fe3+������XӦΪ���������ɽ�Fe2+����Fe3+������NaOH��Һ������ҺpH��������Ŀ����Դ˽����⣬
����Ԫ�ػ��ϼ۴�����Ϊ0������Ԫ�ػ��ϼۣ�
������Al��Fe�Լ�Fe2O3�����ʵ�����ϵ��ȷ��������ȷ����Һ��FeԪ�صĴ����γ��Ƿ���Fe3+�����������ӵ��������ʼ��������ӵĴ��ڣ�
����[AlFe��OH��nCl6-n]m��FeΪ+3�ۣ�����ˮ�������ã������XӦΪ���������ɽ�Fe2+����Fe3+��
��� �⣺�������ϼ���x���ۺ��Ȼ������ɱ�ʾΪ[AlFe��OH��nCl6-n]m���ɴ˺����ڻ��ϼۺ�Ϊ0�ã�3+x-n-��6-n��=0��
x=3������PAFC����Ԫ�صĻ��ϼ�Ϊ+3��
�ʴ�Ϊ��+3��
������Al��Fe�Լ�Fe2O3�����ʵ�����ϵ��ȷ��������ȷ����Һ��FeԪ�صĴ����γ��Ƿ���Fe3+������������Һ�У�����ȷ���Ƿ�һ�����ڵ�������ΪFe3+��Ϊ֤��������ȷʵ���ڣ�ȡ������Һ����KSCN��Һ����Һ��Һ��Ѫ��ɫ��֤������Fe3+��
�ʴ�Ϊ��C��ȡ������Һ����KSCN��Һ����Һ��Һ��Ѫ��ɫ��
����[AlFe��OH��nCl6-n]m��FeΪ+3�ۣ�����ˮ�������ã������XӦΪ���������ɽ�Fe2+����Fe3+����Ӧ�����ӷ���ʽΪ��2Fe2++Cl2�T2Fe3++2 Cl-��
�ʴ�Ϊ����Fe2+����Fe3+��2Fe2++Cl2�T2Fe3++2 Cl-��
���� ���⿼�����������ʵ�ʵ��̽�������ʷ���ķ�����ʵ�鲽������жϣ���Ҫ���������ʵ�����Ӧ�ã��������̷������������������ǽ���ؼ�����Ŀ�Ѷ��еȣ�


 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ե缫���ϡNa2SO4ˮ��Һʱ���ֱ��������μ�һ��ʯ�һ��ʱ�������������Һ����������������Һ��� | |
| B�� | Ϊʹ��ӦCu+2H2O�TCu��OH��2��+H2������������ͭƬ���������缫�����NaClˮ��Һ | |
| C�� | ��ⷨ������ͭʱ��Ӧʹ��ͭ���Դ���������������е������Һ��Cu2+Ũ�Ȳ��� | |
| D�� | ���Ե缫���MgCl2��Һ���ܷ�Ӧ����ʽΪ2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 1 mol Mg ԭ�ӱ�� Mg2+ʱʧȥ�ĵ�����Ϊ2 NA | |
| B�� | ��״���£�11.2 L H2O�����ĵ�����Ϊ5 NA | |
| C�� | ���³�ѹ�£�16g O2 ��16gO3���е�ԭ����Ϊ��ͬ | |
| D�� | 0.1 mol/L K2SO4 ��Һ�к��� K+Ϊ0.2 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 +Br2$\stackrel{Fe}{��}$
+Br2$\stackrel{Fe}{��}$ +HBr��
+HBr���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�
ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�| �Ҵ� | 1��2-�������� | ���� | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
| �ܶ�/g•cm-3 | 0.79 | 2.2 | 0.71 |
| �е�/�� | 78.5 | 132 | 34.6 |
| �۵�/�� | һl30 | 9 | -1l6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com