
| A�� | �кͷ�Ӧ��Ӧ�ȵIJⶨʵ���У������β�����������ɻ���ͭ˿������ⶨ�������к���ֵƫ�� | |
| B�� | ��101kPaʱ��2gH2��ȫȼ������Һ̬ˮ���ų�285.8kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ��2H2��g��+O2��g���T2H2O��l����H=-571.6KJ/mol | |
| C�� | ��0.5molN2��1.5molH2�����ܱ������г�ַ�Ӧ����NH3��g��������19.3kJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��?2NH3��g����H=-38.6KJ/mol | |
| D�� | HCl��NaOH��Ӧ���к��ȡ�H=-57.3KJ/mol����H2SO4��Ca��OH��2��Ӧ�ķ�Ӧ�ȡ�H=-��2��57.3��KJ/mol |
���� A������ͭ˿���������ȣ���ʹ��������ɢʧ��
B�������Ȼ�ѧ����ʽ�ĺ������д�������ش�
C�����ݷ�ӦΪ���淴Ӧ��������ȫ���У�
D��H2SO4��Ca��OH��2��Ӧ��������Ƴ���������������ˮ��
��� �⣺A���кͷ�Ӧ��Ӧ�ȵIJⶨʵ���У������β�����������ɻ���ͭ˿��������ᵼ�²�������ɢʧ����ʹ�ⶨ������¶�ƫ�ͣ���Ӧ����ֵƫС����A����
B����101kPaʱ��2gH2��ȫȼ������Һ̬ˮ���ų�285.8kJ��������2H2��g��ʮ02��g��=2H2O��l����H=-571.6KJ/mol����B��ȷ��
C��0.5mol N2��1.5molH2�����ܱյ������г�ַ�Ӧ����NH3��g��������19.3kJ����ӦΪ���淴Ӧ����1molN2��3molH2�����ܱյ������г�ַ�Ӧ����NH3��g�������Ȳ���38.6kJ�����Ȼ�ѧ��Ӧ����ʽ�еķ�Ӧ����ֵ����C����
D��H2SO4��Ca��OH��2��Ӧ��������Ƴ���������������ˮ���ų��������������H2SO4��Ca��OH��2��Ӧ���к��ȡ�H��2����-57.3��kJ/mol����D����
��ѡB��
���� ������Ҫ�����к��ȡ�ȼ���ȡ����淴Ӧ��֪ʶ��������˫������������õĿ��飬�ѶȲ���ע��ȷ������ظ��ѧϰ��ע����ػ���֪ʶ�Ļ��ۣ�


 ��һ������Ԫͬ�����ؾ�ϵ�д�
��һ������Ԫͬ�����ؾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3��3-�������� | B�� | 3-��-1-��ϩ | ||
| C�� | 2��2-����-1-��ϩ | D�� | 3-��-2-�һ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���� | ���� |
| A | ǿ���������ʿ�������ɱ������ | ClO2����������ˮ���� |
| B | ��Ӧ��Ũ��Խ��Ӧ����Խ�� | �����£���ͬ����Ƭ�зֱ����������Ũ��ϡ���ᣬŨ��������Ƭ���ܽ��� |
| C | �ṹ��������Ƶ����ʣ��е�����Է���������������� | NH3�е����PH3 |
| D | ��ǿ���������ȡ�������� | ����ͨ������ͭ��Һ�в��ܷ�Ӧ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ������ ʵ����� | V��2.0mol/L KNO3��/ mL | �� | |
| 1 | a | �� | |
| 2 | a | �� | |
| 3 | a | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ڢ�B�� | B�� | �������ڢ�B�� | C�� | �������ڢ�B�� | D�� | �������ڢ�B�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| AԪ�صĺ���������͵��Ӳ�����ȣ�Ҳ����������ḻ��Ԫ�أ� |
| BԪ��ԭ�ӵĺ���p��������s��������1�� |
| Cԭ�ӵĵ�һ�����ĵ����ֱܷ��ǣ�I1=738kJ/mol I2=1451J/mol I3=7733kJ/mol I4=10540kJ/mol |
| Dԭ�Ӻ�������p���ȫ��������� |
| EԪ�ص������������������IJ�Ϊ4�� |
| F��ǰ�������е縺����С��Ԫ�أ� |
| G�����ڱ��ĵ����У� |
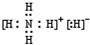 ��
�� ����ͬѧ�����ĵ����Ų�ͼΥ��������ԭ����
����ͬѧ�����ĵ����Ų�ͼΥ��������ԭ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ʯ�Һ��Ȼ�炙�ϼ��� | |
| B�� | �����Թ��е��Ȼ�粒��� | |
| C�� | ����ƿ�е�Ũ��ˮ���� | |
| D�� | ����Һ©���е�Ũ��ˮ����װ�м�ʯ�ҵ���ƿ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com