



 ,C为
,C为 ,B为
,B为 ,A为
,A为 ,由阿莫西林的结构简式,结合E、F的分子式,可知E的结构简式为
,由阿莫西林的结构简式,结合E、F的分子式,可知E的结构简式为 ,F的结构简式为
,F的结构简式为 ,据此解答.
,据此解答. ,C为
,C为 ,B为
,B为 ,A为
,A为 ,由阿莫西林的结构简式,结合E、F的分子式,可知E的结构简式为
,由阿莫西林的结构简式,结合E、F的分子式,可知E的结构简式为 ,F的结构简式为
,F的结构简式为 ,
, ,分子中含氧官能团的名称是:羟基、醚键,
,分子中含氧官能团的名称是:羟基、醚键, ,故答案为:
,故答案为: ;
; ,含氧官能团为羟基和羧基,故答案为:羧基;
,含氧官能团为羟基和羧基,故答案为:羧基; ,在铜催化作用下加热可生成C,反应的方程式为:
,在铜催化作用下加热可生成C,反应的方程式为: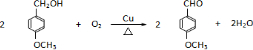 ,由于酚羟基易被氧化,反应①的目的是保护酚羟基不被氧化,
,由于酚羟基易被氧化,反应①的目的是保护酚羟基不被氧化, ;保护酚羟基不被氧化;
;保护酚羟基不被氧化; )的同分异构体,G分子满足下列三个条件:
)的同分异构体,G分子满足下列三个条件: ,
, ;
;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1:2 |
| B、1:1:1 |
| C、4:2:1 |
| D、1:2:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 无标题的正确的名称是( )
无标题的正确的名称是( )| A、3,3-二甲基-4-乙基戊烷 |
| B、3,3-二甲基-2-乙基戊烷 |
| C、3,4,4-三甲基己烷 |
| D、3,3,4-三甲基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 发生的现象 | 解释或结论 |
| A | 将溴乙烷与NaOH乙醇溶液加热产生的气体通入高锰酸钾溶液 | 高锰酸钾溶液颜色变浅 | 不能说明有乙烯产生 |
| B | 将一定量铁粉和铜粉的混合物加入由稀H2SO4和稀HNO3组成的混合溶液中 | 充分反应后,有金属粉末剩余 | 往反应后的溶液中加入足量的稀H2SO4,则金属粉末的质量一定不会减少 |
| C | 将一段用砂纸打磨过的镁条放入盛有热水的试管中 | 镁条表面立即有大量气泡和白色沉淀生成 | 镁和水反应生成了H2和Mg(OH)2 |
| D | 向某溶液中加入BaCl2溶液,再滴加稀硝酸 | 产生白色沉淀 | 则原溶液中含有SO42- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:



 的部分流程图:
的部分流程图:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某实验中,用0.1000mol?L-1标准盐酸测定某NaOH溶液的浓度,其操作步骤如下:
某实验中,用0.1000mol?L-1标准盐酸测定某NaOH溶液的浓度,其操作步骤如下:| 序号 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数V1(mL) | 滴定后读数V2(mL) | ||
| 第一次 | 20.00 | 0.50 | 25.40 |
| 第二次 | 20.00 | 4.00 | 29.10 |
| 第三次 | 20.00 | 5.15 | 30.15 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com