
 .
. 科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ③⑤ | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
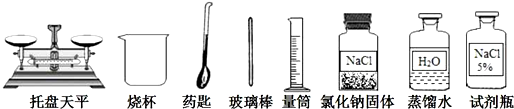
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向盛有二氧化锰的锥形瓶中滴入浓盐酸 | 产生黄绿色气体 | 氧化性:MnO2>Cl2 |
| B | 分别向水和乙醇中投入等质量、等大小的金属钠 | 水中产生气泡较快 | 羟基中氢的活泼性:H2O>乙醇 |
| C | 向滴有KSCN试剂的Fe(NO3)2的溶液中加入盐酸 | 溶液变红 | Fe2+被盐酸氧化为Fe3+ |
| D | 向饱和石灰水中加入Na2O2 | 有白色沉淀析出 | Na2O2与Ca(OH)2反应生成白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
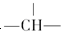 ,则该结构的烃的一氯取代物最多可能有几种(不考虑立体异构)( )
,则该结构的烃的一氯取代物最多可能有几种(不考虑立体异构)( )| A. | 9 | B. | 8 | C. | 7 | D. | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在由水电离产生的氢离子浓度为10-13 mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3-四种离子能大量共存 | |
| B. | 已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)=6.82×10-6 | |
| C. | 对于反应2N2H4(l)=N2(g)+2H2(g),△H=-50.6 kJ?mol-1,它只在高温下自发进行 | |
| D. | 常温下,将0.2 mol?L-1某一元碱(ROH)溶液和0.1 mol?L-1HCl溶液等体积混合,混合后溶液pH<7,则c(ROH)>c(R+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 次氯酸根离子的化学式:ClO- | B. | 干冰的分子式:H2O | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | 乙醇的结构简式:C2H6O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com