
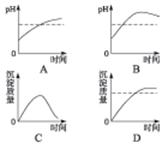
用石墨作电极电解3 mol·L-1 KCl和0.5 mol·L-1 Al2(SO4)3的混合溶液时,下列电解变化的曲线合理的是()
AD
石墨为惰性电极,电解时,溶液中的离子在电极上放电,放电能力为阳离子:H+>Al3+>K+,阴离子:Cl->OH->SO![]() 。电极反应为:阳极,2Cl--2e-
。电极反应为:阳极,2Cl--2e-![]() Cl2↑,阴极,2H++2e-
Cl2↑,阴极,2H++2e-![]() H2↑,溶液中还伴随有如下反应:Al3++3OH-
H2↑,溶液中还伴随有如下反应:Al3++3OH-![]() Al(OH)3↓,其中H+和OH-是由H2O电离产生的,故电解总反应为:2Al3++6Cl-+6H2O
Al(OH)3↓,其中H+和OH-是由H2O电离产生的,故电解总反应为:2Al3++6Cl-+6H2O![]() 2Al(OH)3↓+3H2↑+3Cl2↑
2Al(OH)3↓+3H2↑+3Cl2↑
由于题中已知条件显示n(Al3+)∶n(Cl-)=1∶3,所以电解至Al3+和Cl-恰好消耗完时,溶液为K2SO4溶液,这时若继续电解,则实际电解的是水。溶液由于Al3+水解,pH<7,则电解过程中溶液的pH先升高,后保持不变,图A符合题意。很明显生成Al(OH)3沉淀的量应符合图D。


科目:高中化学 来源:2013届河南省镇平一高高二第一次月考化学试卷(解析版) 题型:选择题
用石墨作电极电解3 mol·L-1 KCl和0.5 mol·L-1 Al2(SO4)3,的混合溶液时,下列电解变化的曲线合理的是 ( )


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com