
 利用如图所示的装置和其他必要的用品,利用反应:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2+3Cu+3H2O证明氨气具有还原性,请回答下列有关问题.
利用如图所示的装置和其他必要的用品,利用反应:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2+3Cu+3H2O证明氨气具有还原性,请回答下列有关问题.分析 (1)依据NH3.H2O?NH3↑+H2O反应特点为吸热反应,利用化学平衡移动理论解答;依据反应物状态与反应条件选择发生装置;
(2)氨气为污染气体,不能直接排放的到空气中,氨气为碱性气体,能够被浓硫酸吸收,氨气极易被浓硫酸吸收,应防止发生倒吸;
(3)氨气与氧化铜如果发生氧化还原反应,生成产物为铜,则黑色的氧化铜变化为红色;无水硫酸铜容易结合水生成五水硫酸铜,常用来检验水的存在;
(4)装置A为氨气还原氧化铜装置,装置B为氨气的制备装置,装置C为尾气处理装置,装置D为氨气干燥装置,据此解答.
解答 解:(1)解:一水合氨中存在平衡NH3.H2O?NH3↑+H2O,且该反应是吸热反应,向浓氨水中加入NaOH固体,氢氧化钠溶解放出热量促进一水合氨分解生成氨气;
反应物氨水为液体,氢氧化钠固体,反应条件不需要加热,所以应选择装置B做发生装置;
故答案为:一水合氨中存在平衡NH3.H2O?NH3↑+H2O,该反应是吸热反应,向浓氨水中加入NaOH固体,氢氧化钠溶解放出热量促进一水合氨分解生成氨气;B;
(2)氨气为污染气体,不能直接排放的到空气中,氨气为碱性气体,能够被浓硫酸吸收,所以C中浓硫酸作用是:吸收过量的氨气防止空气污染,氨气极易被浓硫酸吸收,应防止发生倒吸;
故答案为:吸收过量的氨气防止空气污染;防止发生倒吸;
(3)氨气与氧化铜如果发生氧化还原反应,生成产物为铜,看到现象为:黑色的氧化铜变化为红色;
无水硫酸铜容易结合水生成五水硫酸铜,白色固体变为蓝色,可证明水蒸气的存在;
故答案为:黑色固体变为红色;无水硫酸铜;
(4)依据实验目的制备氨气并检验氨气的还原性,正确的顺序为:制取氨气、干燥氨气、性质检验、尾气吸收,所以正确的顺序为:BDAC;
故答案为:BDAC.
点评 本题考查了氨气的制备和性质的检验,熟悉实验原理及氨气的性质是解题关键,注意每个装置作用的分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1mol任何气体的体积都约为22.4L | |
| B. | 标准状况下,氧气的体积约为22.4L | |
| C. | 在同温同压下,22g CO2与11.2L HCl含有相同的分子数 | |
| D. | 标准状况下,32g氧气的体积约是22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 分子式为C16H18O9 | |
| B. | 能与NaHCO3反应 | |
| C. | 能发生取代反应、氧化反应和消去反应 | |
| D. | 1 mol绿原酸最多与6 mol Br2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,F:CH3CHO.
,F:CH3CHO. ,
, .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ν(H2)=0.03 mol•L-1•min-1 | B. | ν(NH3)=1.7 g•L-1•min-1 | ||
| C. | ν(N2)=0.02 mol•L-1•min-1 | D. | ν(NH3)=0.01 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石英与烧碱反应:SiO2+2OH-═SiO32-+H2O | |
| B. | 硅与烧碱反应:Si+2OH-═SiO32-+H2↑ | |
| C. | 硅酸钠溶液中通入少量CO2:SiO32-+CO2+H2O═CO32-+H2SiO3↓ | |
| D. | 往水玻璃中加入盐酸:2H++SiO32-═H2SiO3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeO、Fe2O3 | B. | FeO、Fe3O4 | C. | Fe2O3、Fe3O4 | D. | FeO、Fe2O3、Fe3O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,
,
 的同分异构体:
的同分异构体: 、
、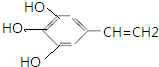 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com