
【题目】下列四种元素中,非金属性最强的是( )
A. Cl B. P C. S D. F
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案科目:高中化学 来源: 题型:
【题目】将燃着的镁条伸入盛有二氧化碳的集气瓶中,镁条继续燃烧,反应的化学方程式为CO2+2Mg ![]() C+2MgO,该反应属于( )
C+2MgO,该反应属于( )
①化合反应 ②分解反应 ③置换反应 ④复分解反应 ⑤氧化还原反应 ⑥离子反应 ⑦非氧化还原反应.
A.①③⑦
B.②③⑥
C.③⑤
D.④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 摩尔质量就等于物质的相对分子质量
B. 摩尔质量等于物质式量(的相对分子质量或的相对原子质量)的6.02×1023倍
C. HNO3的摩尔质量是63g
D. 硫酸和磷酸的摩尔质量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如图1的装置:(以下均假设反应过程中溶液体积不变).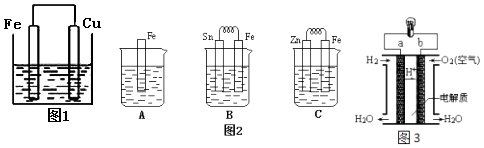
(1)铁片上的电极反应式为 , 铜片周围溶液会出现的现象.
(2)若2min后测得铁片和铜片之间的质量差为1.2g,计算:导线中流过的电子的物质的量为mol;
(3)金属的电化学腐蚀的本质是形成了原电池.如图2所示,烧杯中都盛有稀硫酸.
①图2B中的Sn为极,Sn极附近溶液的pH(填增大、减小或不变) .
②图2C中被腐蚀的金属是 . 比较A,B,C中纯铁被腐蚀的速率由快到慢的顺序是 .
(4)人们应用原电池原理制作了多种电池,以满足不同的需要.燃料电池是一种高效、环境友好的供电装置,如图3是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:
①氢氧燃料电池的总反应化学方程式是: .
②电池工作一段时间后硫酸溶液的浓度(填“增大”、“减小”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 植物油的主要成分是高级脂肪酸B. 醋酸铅溶液可使鸡蛋清中的蛋白质变性
C. 蔗糖及其水解产物均可发生银镜反应D. 合成纤维和棉花的主要成分均为纤维素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究生铁与浓硫酸反应所得溶液和气体的成分,他们将一定量的生铁与浓硫酸混合加热,观察到固体完全溶解,并产生大量气体。实验室现有试剂:0.01mol·L-1酸性KMnO4溶液、0.10mol·L-1KI溶液、新制氯水、淀粉溶液、蒸馏水。
一、提出猜想
I.所得溶液中可能含有Fe2+和Fe3+中的一种或两种:
II.所得气体中能闻到刺激性气味,说明气体中肯定含有_________(填分子式)。
二、实验探究
目的 | 实验操作 | 预期现象 | 结论 |
验证I | 步骤①:取少量酸性KMnO4溶液,滴入所得溶液中 | a____________ | 含有Fe2+ |
步骤②:b__________ | C__________________ | 含有Fe3+ | |
验证II | 将所得气体通入如下装置:
| d__________________ | 含有两种或两种以上气体 |
三、问题讨论
(1)有人提出:若选用KSCN溶液和新制氯水就可以完成猜想I的所有探究,这种方法是否可行?_____________(填“可行”或“不可行”)原因是_____________________。
(2)有人提出:试管中的气体可能是H2和X,为此设计了如下实验装置(图中夹持仪器已省略)。
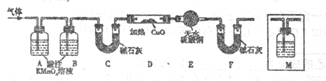
气体X产生的原因是(用化学方程式表示)___________________________________。
②为了验证X的存在,M中盛放的试剂为___________,并将M置于______(选填序号)。
a.A之前 b.A-B间 c.B-C间 d.C-D间
③气体中存在X的实验现象是_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4(s)+CO(g)![]() MgO(s)+SO2(g)+ CO2(g) ΔH>0,该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
MgO(s)+SO2(g)+ CO2(g) ΔH>0,该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是

选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+3B(g)![]() 2C(g),△H=-QkJ/mol有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 mol A和3 mol B,在一定条件下达到平衡时放出热量为Q1kJ;在相同的条件下,向乙容器中加入2 mol C达到平衡后吸收热量为Q2kJ;已知Q1=3Q2。下列叙述不正确的是
2C(g),△H=-QkJ/mol有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 mol A和3 mol B,在一定条件下达到平衡时放出热量为Q1kJ;在相同的条件下,向乙容器中加入2 mol C达到平衡后吸收热量为Q2kJ;已知Q1=3Q2。下列叙述不正确的是
A. 甲中A的转化率为75%
B. Q1+Q2=Q
C. 达到平衡后,再向乙中加入0.25 mol A、0.75 mol B、1.5 mol C,平衡向正反应方向移动
D. 乙中的热化学方程式为2C(g)![]() A(g)+3B(g) ΔH=+Q2kJ/mol
A(g)+3B(g) ΔH=+Q2kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com