
| A. | 氢化锂是一种电解质 | B. | LiH是离子晶体[ | ||
| C. | LiH是一种强氧化剂 | D. | LiH中Li+半径小于H-半径 |
分析 A.在水溶液中或熔融状态下能导电的化合物为电解质;
B.LiH中存在离子键;
C.根据H元素的化合价分析;
D.电子排布相同的离子,原子序数越大,离子半径越小.
解答 解:A.在水溶液中或熔融状态下能导电的化合物为电解质,由于氢化锂在熔融时能导电,故为电解质,故A正确;
B.LiH中锂离子与氢离子之间以离子键结合,属于离子晶体,故B正确;
C.LiH中H元素的化合价为-1价,具有最低价,具有还原性,所以LiH是一种还原剂,故C错误;
D.电子排布相同的离子,原子序数越大,离子半径越小,所以LiH中H-半径大于Li+半径,故D正确.
故选C.
点评 本题考查了化学键、氧化还原反应、离子半径的比较等,题目难度不大,侧重于基础知识的考查,注意相关知识的积累.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:计算题
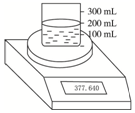 如图所示测定Na2O2(含Na2O杂质)纯度的实验装置,不同时间电子天平的读数如列表所示:
如图所示测定Na2O2(含Na2O杂质)纯度的实验装置,不同时间电子天平的读数如列表所示:| 实验操作 | 时间/s | 电子天平读数/g |
| 烧杯+水 | 370.000 | |
| 烧杯+水+样品 | 0 | 377.640 |
| 30 | 376.920 | |
| 60 | 376.400 | |
| 90 | 376.200 | |
| 120 | 376.200 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
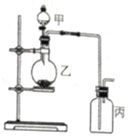 利用如图所示装置进行实验,能实现实验目的是(必要时可加热)( )
利用如图所示装置进行实验,能实现实验目的是(必要时可加热)( )| 选项 | 实验目的 | 甲 | 乙 | 丙 |
| A | 制取并收集NO2 | 浓硝酸 | 铜片 | 水 |
| B | 制取并验证SO2具有漂白性 | 70%硫酸 | 亚硫酸钠 | 品红溶液 |
| C | 制取并验证氯气没有漂白性 | 浓盐酸 | 二氧化锰 | 干燥的红布条 |
| D | 比较HCl、H2CO3和H2SiO3酸性的强弱 | 盐酸 | 大理石 | 硅酸钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
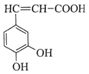 咖啡酸(如图)存在于野胡萝卜、光叶水苏、荞麦等物中.咖 啡酸有止血作用,特别对内脏的止血效果较好.A是咖啡酸的同分异构体,其苯环上只有1个取代基,1molA能与2molNaHCO3反应,A的结构简式C6H5CH(COOH)2.
咖啡酸(如图)存在于野胡萝卜、光叶水苏、荞麦等物中.咖 啡酸有止血作用,特别对内脏的止血效果较好.A是咖啡酸的同分异构体,其苯环上只有1个取代基,1molA能与2molNaHCO3反应,A的结构简式C6H5CH(COOH)2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 关于有机物A的说法不正确的是( )
关于有机物A的说法不正确的是( )| A. | A的分子式为C16H1403 | |
| B. | A可使酸性KMnO4溶液褪色和溴水褪色 | |
| C. | A苯环上的一氯代物同分异构体有2种 | |
| D. | A既可发生氧化反应和加成反应,又可以发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操 作 | 现 象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸只表现脱水性 |
| B | 常温下将Al片放入浓硝酸中 | 无明显现象 | Al与浓硝酸不反应 |
| C | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
| D | 将盐酸滴入Na2CO3溶液中 | 产生气泡 | Cl的非金属性比C强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com