
【题目】一定温度下,在一容积不变的密闭容器中发生的可逆反应2X(g)![]() Y(g)+Z(s),以下不能作为反应达到平衡标志的是( )
Y(g)+Z(s),以下不能作为反应达到平衡标志的是( )
A.v正(X)=2v逆(Y)B.混合气体的压强不再变化
C.混合气体的密度不再变化D.单位时间内生成lmolY的同时分解2mol X
科目:高中化学 来源: 题型:
【题目】常温下,向20 mL 0.2 mol·L-1二元酸H2A溶液中滴加0.2 mol·L-l NaOH溶液,有关微粒物质的量变化如图。下列叙述正确的是( )
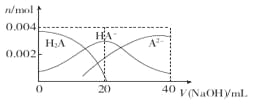
A. 当V(NaOH)="20" mL时,溶液中各离子浓度的大小顺序为:c(Na+)>c(HA-)>c( A2-)>c( OH-)> ((H+)
B. 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水中的大
C. 等浓度H2A和NaHA的混合溶液中无论加入少量的强酸或强碱,溶液的pH变化都不大
D. 当V(NaOH) ="40" mL时,升高温度,c(Na+)/c(A2-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.实验室用锌与稀硫酸反应时,滴加少量硫酸铜溶液能加快反应速率,因为硫酸铜是催化剂
B.某温度下,一定体积的密闭容器中进行可逆反应:![]() ,平衡后加入一定量X,则
,平衡后加入一定量X,则![]() 增大
增大
C.温度和压强一定时,对于可逆反应:![]() ,混合气体的密度不再改变,则反应达到平衡状态
,混合气体的密度不再改变,则反应达到平衡状态
D.将![]() 溶液与
溶液与![]() 溶液混合后生成白色沉淀,是两种溶液水解相互促进的结果
溶液混合后生成白色沉淀,是两种溶液水解相互促进的结果
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧锂离子电池的正极材料试样![]() 主要含有
主要含有![]() 及少量Al、Fe等
及少量Al、Fe等![]() 可通过下列实验方法回收钴、锂.
可通过下列实验方法回收钴、锂.
(1)在上述溶解过程中,![]() 被氧化成
被氧化成![]() ,
,![]() 在溶解过程中反应的离子方程式为 ______ .
在溶解过程中反应的离子方程式为 ______ .
沉淀物 | 开始沉淀pH | 沉淀完全pH |
|
|
|
|
|
|
|
|
|
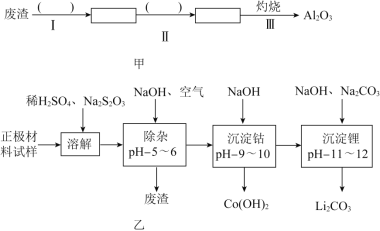
(2)除杂时通入空气的目的 ______ ,所得的废渣成分为 ______ ![]() 从废渣中获得
从废渣中获得![]() 的部分流程如图甲所示,括号表示加入的试剂,方框表示所得到的物质.则步骤I需要的玻璃仪器有 ______ ,步骤Ⅱ中反应的离子方程式是 ______ .
的部分流程如图甲所示,括号表示加入的试剂,方框表示所得到的物质.则步骤I需要的玻璃仪器有 ______ ,步骤Ⅱ中反应的离子方程式是 ______ .
(3)工业上,将![]() 粗品制备成高纯
粗品制备成高纯![]() 的部分工艺如图乙.
的部分工艺如图乙.
![]() 将
将![]() 溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解.
溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解.
![]() 电解后向LiOH溶液中加入过量
电解后向LiOH溶液中加入过量![]() 溶液,过滤、烘干得高纯
溶液,过滤、烘干得高纯![]() .
.
①![]() 中,阴极的电极反应式是 ______ .
中,阴极的电极反应式是 ______ .
②![]() 中,生成
中,生成![]() 反应的化学方程式是 ______ .
反应的化学方程式是 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.常温下,反应![]() 能自发进行,则该反应的
能自发进行,则该反应的![]()
B.浑浊的苯酚试液中加入饱和![]() 溶液变澄清,则酸性:苯酚
溶液变澄清,则酸性:苯酚![]() 碳酸
碳酸
C.铅蓄电池在放电过程中,负极质量减少,正极质量增加
D.用饱和![]() 溶液处理
溶液处理![]() 沉淀,可将
沉淀,可将![]() 转化为
转化为![]() ,说明
,说明![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mL0.1mol·L-1CuCl2溶液中滴入0.1ml·L-1的Na2S溶液,滴加过程中溶液中-1gc(Cu2+)随滴人的Na2S溶液体积的变化如图所示。下列叙述正确的是
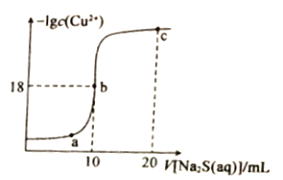
A. Na2S溶液中:c(S2-)+c(HS-)+c(H2S)==2c(Na+)
B. Ksp(CuS)的数量级为10-36
C. a、b、c三点溶液中,b点水的电离程度最大
D. c点溶液中:c(C1-)=2c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,对应的现象以及解释或结论都正确且两者具有因果关系的是
选项 | 实验 | 现象 | 解释或结论 |
A | 向足量的浓硝酸中加入铁片,一段时间后加入铜粉 | 有气体生成,溶液呈蓝绿色 | 浓硝酸将Fe氧化为 |
B | 分别向 | 均有白色沉淀产生 | 金属性: |
C | 表面变黑的银器浸泡到盛有食盐水的铝制容器中,银器与铝接触 | 银器变得光亮如新 | 构成原电池,铝做负极,硫化银得电子被还原成单质银 |
D | 向 | 白色沉淀逐渐变为浅蓝色 |
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)Al(OH)3酸式电离方程式:___________________________________
(2)用离子方程式分析Na2CO3溶液显碱性的主要原因:___________________________________
(3)CaCO3沉淀溶解平衡方程式:_____________________________________
(4)25℃时,四种溶液 ① pH=2的H2SO4溶液、②pH=12的Ba(OH)2溶液,③pH=4的NH4Cl溶液,④pH=12的CH3COONa溶液,水电离的c(H+)之比是______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.Ksp(AB2)小于Ksp(CD),说明AB2的溶解度一定小于CD的溶解度
B.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
C.2C+SiO2![]() Si+2CO↑,此反应能够进行是因为碳的还原性比硅强
Si+2CO↑,此反应能够进行是因为碳的还原性比硅强
D.弱酸也可以通过复分解反应制强酸,如:H2S+CuSO4=H2SO4+CuS↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com