
室温下,用0.100 mol·L-1 NaOH溶液分别滴定20.00 mL 0.100 mol·L-1 的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是( )
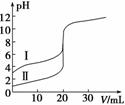
A.Ⅱ表示的是滴定醋酸的曲线
B.pH=7时,滴定醋酸消耗的V(NaOH)小于20 mL
C.V(NaOH) =20.00 mL时,两份溶液中c(Cl-)=c(CH3COO-)
D.V(NaOH) =10.00 mL时,醋酸溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
科目:高中化学 来源: 题型:
科学家一直致力于研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、N2压力1.0×105 Pa、反应时间3 h):
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 | 2.0 |
相应的热化学方程式如下:
N2(g)+3H2O(l)===2NH3(g)+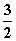 O2(g)
O2(g)
ΔH=765.2 kJ·mol-1
回答下列问题:
(1)请画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化示意图,并进行必要标注。
(2)与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议:
________________________________________________________________________
________________________________________________________________________。
(3)工业合成氨的反应为N2(g)+3H2(g)
 2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为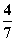 。计算:
。计算:
①该条件下N2的平衡转化率;
②该条件下反应2NH3(g)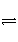
 N2(g)+3H2(g)的平衡常数。
N2(g)+3H2(g)的平衡常数。
查看答案和解析>>
科目:高中化学 来源: 题型:
将Ca(OH)2加入蒸馏水中,一段时间后达到沉淀溶解平衡:Ca(OH)2(s)Ca2+(aq)+2OH-(aq)。下列说法中正确的是( )
A.恒温下向溶液中加CaO,溶液的pH升高
B.给溶液加热,溶液的pH升高
C.恒温下向溶液中加CaO后,溶液中的n(OH-)减小
D.向溶液中加入少量的NaOH固体,Ca(OH)2固体的质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
pC类似pH,是指极稀溶液中,溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为1×10-3 mol·L-1,则该溶液中溶质的pC=-lg(1×10-3)=3。下图为H2CO3在加入强酸或强碱溶液溶液后,平衡时溶液中三种成分的pC—pH图。请回答下列问题:
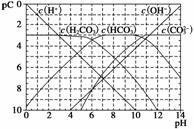
(1)在人体血液中,HCO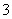 能起到使人体血液pH保持在7.35~7.45的作用。
能起到使人体血液pH保持在7.35~7.45的作用。
①请用电解质溶液中的平衡解释:__________________(用离子方程式表示)。
②正常人体血液中,HCO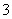 的水解程度________电离程度(填“<”、“>”或“=”)。
的水解程度________电离程度(填“<”、“>”或“=”)。
③pH=7.00的血液中,c(H2CO3)________c(HCO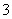 )(填“<”、“>”或“=”)。
)(填“<”、“>”或“=”)。
(2)H2CO3一级电离平衡常数的数值Ka1≈________。
(3)某同学认为该溶液中Na2CO3的水解是微弱的,发生水解的CO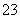 不超过其总量的10%。请你设计简单实验证明该同学的观点是否正确______________________。
不超过其总量的10%。请你设计简单实验证明该同学的观点是否正确______________________。
(4)已知某温度下Li2CO3的Ksp为1.68×10-3,将适量Li2CO3固体溶于100 mL水中至刚好饱和,饱和Li2CO3溶液中c(Li+)=0.15 mol·L-1、c(CO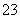 )=0.075 mol·L-1。若t1时刻在上述体系中加入100 mL 0.125 mol·L-1 Na2CO3溶液,列式计算说明是否有沉淀产生。
)=0.075 mol·L-1。若t1时刻在上述体系中加入100 mL 0.125 mol·L-1 Na2CO3溶液,列式计算说明是否有沉淀产生。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25 ℃时,H2CO3的K1=4.4×10-7,K2=4.7×10-11,NH3·H2O的K=1.75×10-5。下列有关0.1 mol·L-1的(NH4)2CO3、NH4HCO3溶液的说法中正确的是(双选)( )
A.NH4HCO3溶液呈中性
B.(NH4)2CO3溶液呈碱性
C.(NH4)2CO3溶液中,c(NH )+c(NH3·H2O)=2[cCO
)+c(NH3·H2O)=2[cCO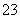 )+c(HCO
)+c(HCO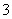 )+c(H2CO3)]
)+c(H2CO3)]
D.等物质的量浓度的两种溶液中的NH 浓度:前者一定是后者的2倍
浓度:前者一定是后者的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,向盛有1 L 0.1 mol·L-1 NaHSO4溶液的烧杯中不断滴加0.05 mol·L-1的Ba(OH)2溶液,溶液中产生沉淀物质的量n(mol)与溶液pH的变化情况如下图所示,下列说法不正确的是(双选)( )

A.A点时pH=1
B.恰好完全沉淀时Ba(OH)2的体积为2 L
C.B点时,溶液中的离子浓度关系为c(Na+)>c(SO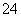 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
D.C点时pH=14
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.天然气、石油都是清洁的可再生能源
B.在燃煤中添加碳酸钙或生石灰可以减少SO2的排放
C.在AgCl饱和溶液中加入AgNO3溶液,达平衡时,溶液中Ksp(AgCl)降低
D.地沟油和矿物油都属于酯类物质
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,有下列四种溶液:
| ① | ② | ③ | ④ |
| 0.1 mol·L-1 NaOH溶液 | pH=11 NaOH溶液 | 0.1 mol·L-1 CH3COOH溶液 | pH=3 CH3COOH溶液 |
下列说法正确的是(双选)( )
A.由水电离出的c(H+):③>①
B.③稀释到原来的100倍后,pH与④相同
C.①与③混合,若溶液pH=7,则V(NaOH)>V(CH3COOH)
D.②④混合,若溶液显酸性,则所得溶液中离子浓度可能为c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是(双选)( )
A.FeCl3、Na2O2、CuS均可由相应单质直接化合生成
B.向稀硫酸中加入铜粉,铜粉不溶解,再加入KNO3固体,铜粉溶解
C.“溶洞”的形成过程中发生了碳酸钙与水、CO2的反应
D.氢氧化铝、碳酸铵能与盐酸反应,不能与氢氧化钠溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com