
【题目】我国稀土资源丰富。下列有关稀土元素![]() Sm与
Sm与![]() Sm的说法正确的是( )
Sm的说法正确的是( )
A. ![]() Sm与
Sm与![]() Sm互为同位素 B.
Sm互为同位素 B. ![]() Sm与
Sm与![]() Sm的质量数相同
Sm的质量数相同
C. ![]() Sm与
Sm与![]() Sm是同一种核素 D.
Sm是同一种核素 D. ![]() Sm与
Sm与![]() Sm的核外电子数和中子数均为62
Sm的核外电子数和中子数均为62
科目:高中化学 来源: 题型:
【题目】下列操作中,能使电离平衡的是H2O![]() H++OH-向右移动且溶液呈酸性的是( )
H++OH-向右移动且溶液呈酸性的是( )
A. 向水中加入NaHSO4溶液 B. 向水中加入Al2(SO4)3固体
C. 向水中加入Na2CO3溶液 D. 将水加热到100℃,使pH=6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:则下列说法正确的是
①CO(g)+![]() O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
②H2(g)+![]() O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1

A. H2的燃烧热为241.8kJ·mol-1
B. 由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g) ΔH =-41.2kJ·mol-1
C. H2(g)转变成H2O(g)的化学反应一定要释放能量
D. 根据②推知反应H2(g) +1/2O2(g)=H2O(l):ΔH>-241.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意回答问题:
(1)中和热的测定所需的玻璃仪器有:大小烧杯、量筒、温度计、 ;
已知:0.55 mol·L-1 HCl和0.50 mol·L-1的NaOH溶液各50 mL反应放出热量为1.42kJ,写出该反应的中和热的热化学方程式: 。
(2)101kpa时,1克乙醇(CH3CH2OH)液体完全燃烧生成稳定氧化物放出热量akJ,写出乙醇燃烧热的热化学方程式: 。
(3)已知H-H、O=O和O-H键的键能分别为436 kJ/mol、498 kJ/mol和463 kJ/mol,2H2O(g) = 2H2(g)+ O2(g) ΔH2= 。
(4)用CO2和氢气合成CH3OCH3(甲醚)是解决能源危机的研究方向之一。
已知:CO(g)+2H2(g ![]() CH3OH(g) ΔH=-90.7 kJ·mol-1
CH3OH(g) ΔH=-90.7 kJ·mol-1
2CH3OH(g ![]() CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CO(g)+H2O(g ![]() CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
则CO2和氢气合成CH3OCH3(g)的热化学方程式为: 。
(5)① 25℃时,浓度均为0.1 mol/L的①氨水②氢氧化钠溶液③盐酸溶液④醋酸溶液,其c(H+)由大到小排列的顺序为: (用序号填空)。
② 95℃时,水中的H+的物质的量浓度为10-6 mol·L-1,若把0.01 mol的NaOH固体溶解于95℃水中配成1 L溶液,则溶液的pH为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是()
A.由于水中存在氢键,所以水很稳定
B.能与酸反应生成盐和水的氧化物一定是碱性氧化物
C.Na2O2中既含有离子键,又含有非极性键
D.由于C=O键是极性键,所以CO2 是极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请回答有关问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
4 | ⑨ | ⑩ |
(1)表中最活泼的金属元素是____(填写元素符号,以下同),非金属性最强的元素是_____;
(2)③与④的最高价氧化物对应水化物的碱性较弱的是__________(填写化学式)。
(3)工业制取⑤的单质的化学反应方程式为:____________________。⑤的气态氢化物在空气中燃烧生成两种氧化物,写出该反应的化学方程式:______________。
(4)写出一个能比较⑦、⑩单质氧化性强弱的离子方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质性质的说法正确的是( )
A.通常状况下,NO2是无色的气体
B.SO2能漂白品红等物质,说明SO2有氧化性
C.氯化钙溶液和AgNO3溶液混合有白色沉淀产生
D.加热时,铁单质与浓硝酸不发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有0.1 mol·L-1醋酸溶液10 mL,加蒸馏水稀释到1 L后,下列变化中正确的是
①电离程度增大 ②c(CH3COOH)增大 ③CH3COO-数目增多 ④c(H+)增大
⑤导电性增强 ⑥![]() 增大 ⑦c(OH-)增大
增大 ⑦c(OH-)增大
A.①②③⑦ B.①③⑤⑥ C.①③⑥⑦ D.②④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】作催熟剂的物质除乙烯外,还有氯酸镁。实验室制备少量氯酸镁晶体【Mg(ClO3)2·6H2O】的流程如下:
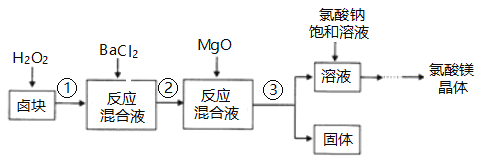

(1)步骤③的操作名称是___________,该步分离出的固体中含有多种成分,任写出一种成分的化学式____________________。
(2)用双氧水溶解卤块,H2O2的主要作用是___________________。
(3)加入饱和氯酸钠溶液发生的主要反应的反应类型是_________________(填四大基本反应类型)。
(4)若卤块中MgCl2·6H2O含量为81.2%,用10L饱和氯酸钠溶液(其中溶质利用率为90%),理论上可以制得氯酸镁晶体的质量是___________(用带a的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com