
| A、铅蓄电池放电时,正极和负极的电极质量均增大 |
| B、反应Cl2(g)+H2O(1)=HCl(aq)+HClO(aq)在常温下能自发进行,则该反应的△H>0 |
| C、加热Fe2(SO4)3溶液,Fe3+的水解程度和溶液的pH均增大 |
| D、C2H5Br水解生成乙醇(△H>0),加入少量NaOH浓溶液并加热,该化学反应速率增大其平衡常数不变 |


科目:高中化学 来源: 题型:
| A、c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| B、c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| C、c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D、c(NH4+)+c(H+)=c(Cl-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
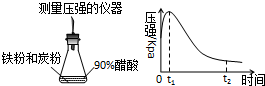 用测量压强的仪器测定生铁在90%醋酸溶液中发生腐蚀的装置及容器内压强随时间变化如图所示,下列分析错误的是( )
用测量压强的仪器测定生铁在90%醋酸溶液中发生腐蚀的装置及容器内压强随时间变化如图所示,下列分析错误的是( )| A、0~t1,可能发生了析氢腐蚀压强增大 |
| B、0~t1,可能反应放热温度升高压强增大 |
| C、t2时压强小于起始压强,一定发生了吸氧腐蚀 |
| D、整个过程中铁粉发生了还原反应生成Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、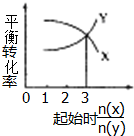 一定条件下,X和Y反应生成Z,由图1推出该反应的方程式可表示为:X+3Y?Z |
B、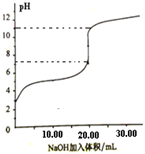 表示NaOH溶液滴加到0.1 mol/L的一元酸溶液得到的滴定曲线(常温下),该实验最好选取酚酞作指示剂 |
C、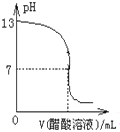 常温下,向NaOH溶液中逐滴加入等浓度的醋酸溶液,所得滴定曲线如图所示.当7<pH<13时,溶液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
D、 用硝酸银溶液滴定等浓度的A-、B-、C-的混合溶液(均可以与Ag+反应生成沉淀),由图可确定首先沉淀的是C- |
查看答案和解析>>
科目:高中化学 来源: 题型:
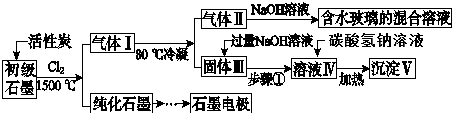
查看答案和解析>>
科目:高中化学 来源: 题型:
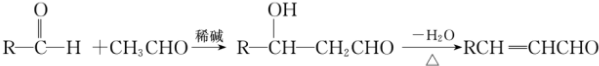
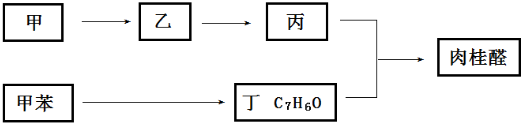

查看答案和解析>>
科目:高中化学 来源: 题型:
| 品 名 | 浓苹果汁 |
| 配 料 | ①浓缩苹果汁 ②蔗糖 ③柠檬黄 ④山梨酸钾 |
| 果汁含量 | ≥80% |
| 生产日期 | 标于包装封口处 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com