


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、做化学实验时产生的废液应倒入废液缸里 |
| B、熄灭酒精灯时,用嘴吹灭 |
| C、炒菜时油锅着火,立即盖上锅盖 |
| D、误食重金属盐,应喝豆浆、牛奶或鸡蛋清等解毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 装置可用于测定中和热 |
B、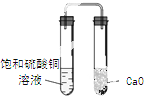 装置久置后,饱和硫酸铜溶液可能析出蓝色晶体 |
C、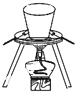 装置在胆矾中结晶水的测定实验中用于灼烧胆矾 |
D、 装置可用于吸收易溶于水的尾气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)有如图所示A、B、C、D四种仪器:请选择下列仪器名称的序号,填入相应的空格内:
(1)有如图所示A、B、C、D四种仪器:请选择下列仪器名称的序号,填入相应的空格内:查看答案和解析>>
科目:高中化学 来源: 题型:
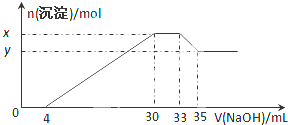 在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.下列叙述正确的是( )
在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.下列叙述正确的是( )| A、x与y的差值为0.1mol |
| B、原溶液中c(Cl-)=0.75 mol?L-1 |
| C、原溶液的c(H+)=0.1 mol?L-1 |
| D、原溶液中n(Mg2+):n(Al3+)=5:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
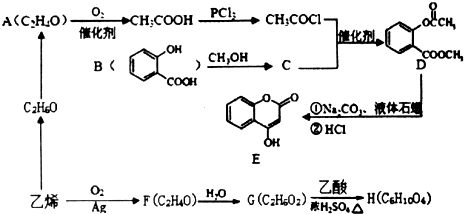
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+ |
| B、Al3+ |
| C、Cu2+ |
| D、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| A、2:1 | B、1:2 |
| C、1:1 | D、2:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com