
在2 L密闭容器内,800℃时反应2NO(g)+O2(g) ====2NO2(g)体系中,n(NO)随时间的变化如下表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)上述反应 (填“是”或“不是”)可逆反应,在第5 s时,NO的转化率为 。
(2)如图中表示NO2变化曲线的是 。用O2表示0~2 s内该反应的平均速率v= 。
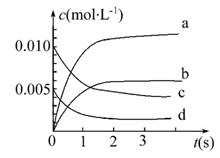
(3)能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
【解析】(1)反应物NO在3 s后剩余0.007 mol,并且不再变化,说明反应达到了平衡状态,此反应一定是可逆反应。NO的转化率为[(0.020 mol-0.007 mol)÷0.020 mol]×100%=65%。
(2)由平衡体系2NO(g)+O2(g) 2NO2(g)可知,NO2为生成物,在0 s时,c(NO2)=
2NO2(g)可知,NO2为生成物,在0 s时,c(NO2)=
0 mol·L-1,随着反应的进行,c(NO2)逐渐增大,当达到平衡时,c(NO2)达到最大值。参加反应的NO的物质的量为0.020 mol-0.007 mol=0.013 mol,根据方程式,参加反应的NO的物质的量等于生成的NO2的物质的量,故平衡时c(NO2)=0.013 mol÷2 L=0.006 5 mol·L-1,故表示NO2变化曲线的为b。0 s~2 s内,v(NO)=
(0.020 mol-0.008 mol)÷2 L÷2 s=0.003 mol·L-1·s-1,故v(O2)= v(NO)=
v(NO)=
0.001 5 mol·L-1·s-1。
(3)a项中未指明正、逆反应速率,故无法说明该反应是否达到平衡状态;由于该反应是前后气体体积不相等的反应,当容器内压强保持不变时,说明该反应已达到平衡状态,b项正确;c项中说明正、逆反应速率相等,故说明该反应已达到平衡状态;由于气体总质量不变,气体总体积也不变,因此,无论该反应是否达到平衡,容器内密度总保持不变,故d项无法说明该反应是否达到平衡状态。
答案:(1)是 65% (2)b 0.001 5 mol·L-1·s-1
(3)b、c


科目:高中化学 来源: 题型:
最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物A,其结构如下:
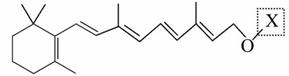
在研究其性能的过程中,发现结构片段X对化合物A的性能起了重要作用。为
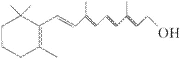 了研究X的结构,将化合物A在一定条件下水解只得到B( )
了研究X的结构,将化合物A在一定条件下水解只得到B( )
和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应____________。
A.取代反应 B.加成反应
C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式____________。
(3)化合物C能经下列反应得到G(分子式为C8H6O2,分子内含有五元环);
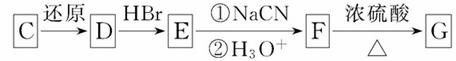
已知:RCOOH RCH2OH,RX
RCH2OH,RX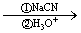 RCOOH
RCOOH
①确认化合物C的结构简式为_______________________________________。
②F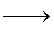 G反应的化学方程式为______________________________________。
G反应的化学方程式为______________________________________。
③化合物E有多种同分异构体,1H核磁共振谱图表明,其中某些同分异构体含有苯环,且苯环上有两种不同化学环境的氢,写出这些同分异构体的结构简式:_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
卤代烃广泛用于化工生产,下列关于卤代烃的说法正确的是( )
A.卤代烃性质稳定,不会对环境造成破坏
B.卤代烃均难溶于水
C.卤代烃都能发生消去反应
D.有小分子(如水)生成的反应是消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
设C+CO2 2CO(正反应吸热),反应速率为v1;N2+3H2
2CO(正反应吸热),反应速率为v1;N2+3H2 2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1和v2的变化情况为 ( )
2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1和v2的变化情况为 ( )
A.同时增大 B.同时减小
C.v1增加,v2减小 D.v1减小,v2增大
查看答案和解析>>
科目:高中化学 来源: 题型:
对于可逆反应M+N Q达到平衡时,下列说法正确的是 ( )
Q达到平衡时,下列说法正确的是 ( )
A.M、N、Q三种物质的浓度一定相等
B.M、N全部变成了Q
C.反应物和生成物的浓度都保持不变
D.反应已经停止
查看答案和解析>>
科目:高中化学 来源: 题型:
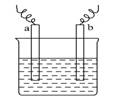
如图中,两电极上发生的电极反应如下:
a极:Cu2++ 2e-====Cu;
b极:Fe-2e-====Fe2+,则以下说法中不正确的是( )
A.该装置一定是原电池
B.a极上一定发生还原反应
C.a、b可以是同种电极材料
D.该过程中能量的转换可以是电能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置示意图如下:
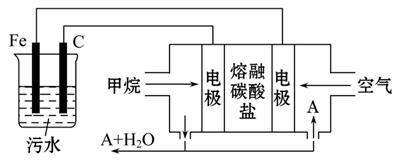
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的________。
a.BaSO4 b.CH3CH2OH c.Na2SO4 d.NaOH
(2)电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应式分别是
Ⅰ.________________________________________________________________;
Ⅱ.________________________________________________________________。
(3)电极反应Ⅰ和Ⅱ的生成物反应得到Fe(OH)3沉淀的离子方程式是________
__________________________________________________________。
(4)该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料作电极。为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见上图)。A物质的化学式是___
___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在用锌片、铜片和稀硫酸组成的原电池装置中,经过一段时间工作后,下列说法中正确的是 ( )
A.锌片是正极,铜片上有气泡产生
B.电流方向是从锌片流向铜片
C.溶液中H2SO4的物质的量减少
D.电解液的pH保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
对于碳骨架如下的4种烃,下列描述不正确的是
( )
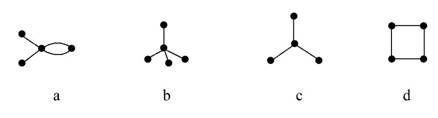
A.a和d是同分异构体
B.b和c是同系物
C.a和d都能发生加成反应
D.b和c、d都能发生取代反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com